1. INTRODUCCIÓN
El reconocimiento molecular es la base de la química supramolecular, facilitando la combinación selectiva de determinadas moléculas. Pedersen, Cram y Lehn fueron galardonados con el Premio Nobel de Química en 1987 por el desarrollo del concepto de “química supramolecular”, que se define como “la química mas allá de las moléculas”, una expresión en cierto modo misteriosa por hacer referencia al más allá. Si consideramos que la química supramolecular se ocupa del estudio de las supramoléculas, definiremos a éstas como entidades grandes y complejas formadas por otras moléculas que interaccionan entre sí a través de enlaces de hidrógeno, interacciones hidrofóbicas y enlaces de coordinación, que siendo débiles, al ser numerosas producen entidades robustas. Este fenómeno es lo que se denomina “efecto Gulliver”, por analogía con el uso de muchas cuerdas diminutas para atar a un gigante cuando el protagonista es capturado en la costa de Lilliput. El estudio de las interacciones no covalentes y su eficacia en la estabilidad de entidades macromoleculares ha sido y es crucial en los distintos ámbitos de la química (1). Las experiencias de reconocimiento molecular de cationes por éteres corona (Pendersen, 1967), el reconocimiento molecular entre moléculas “host-guest” demostrando que ciertas moléculas pueden “acomodar” a otras fue propuesto por Cram y mas tarde en 1978 Lehn propuso el término de química supramolecular. Así, las enzimas actúan como “host” y reconocen molecularmente a sus sustratos “guest” dando lugar a una reacción específica en un bolsillo de la enzima. En 2016, Sauvage, Stoddardt y Feringa recibieron el premio Nobel de Química por sus trabajos en el diseño y síntesis de maquinas moleculares capaces de organizarse y autoensamblarse de manera autónoma mediada por luz o electrones.
Las entidades supramoleculares poseen cualidades y funciones diferentes de las moléculas de partida y que responden mucho más que a las suma de las propiedades de las moléculas individuales. En términos deportivos podemos asimilar las supramoléculas a los equipos deportivos, y así, un buen equipo se define porque es mucho más que la suma de las individualidades que lo componen (2,3). La química supramolecular es la base para numerosas aplicaciones en síntesis, catálisis, separaciones quirales, sensado, señalización, vehiculización y trasporte de fármacos. Ciertas supramoléculas pueden combinarse y auto-ensamblarse dando lugar a entidades con geometría y topología exclusiva (fullerenos, nanotubos de carbono, rotaxanos y catenanos,…) y de este modo una molécula pequeña incluida en un nanotubo como el que forman las ciclodextrinas puede experimentar isomerización cis–trans por absorción de energía asociada a radiación electromagnética en la región de los 600 nm (NIR) en condiciones suaves que evitan su degradación por vía fotoquímica.
2. CAVITANDOS
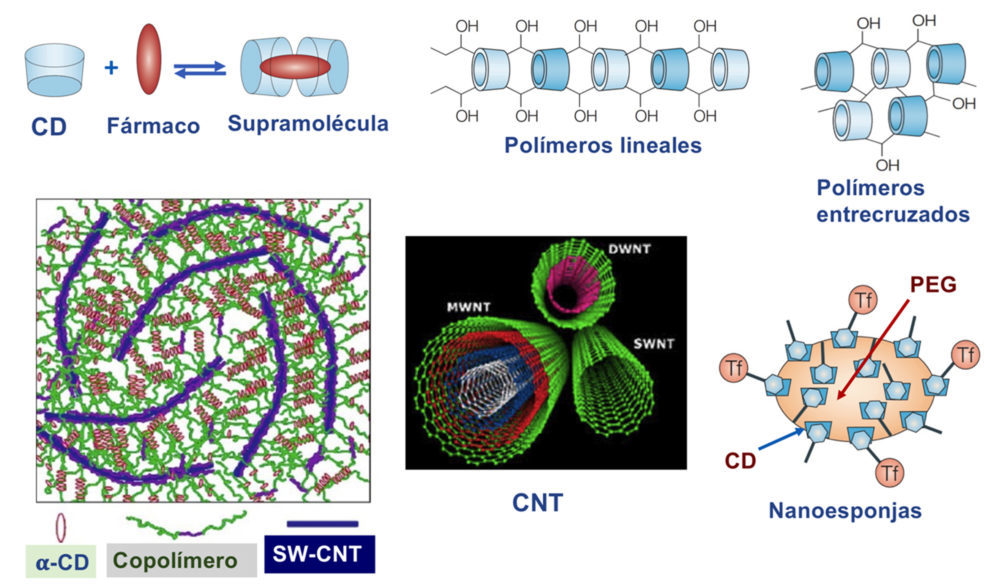
Se denominan cavitandos al conjunto de supramoléculas que poseen una cavidad central capaz de reconocer y alojar en su interior una variedad de especies, desde cationes, como por ejemplo los éteres corona, que tienen por modelo un cavitando de origen natural como son las porfirinas, hasta los mas sofisticados nanotubos de carbono. También son de origen natural las ciclodextrinas (4) y, utilizándolas como modelo, se han diseñado los calixarenos y los cucurbiturilos (5), así denominados por su forma de calabaza y que están formados por unidades de glicolurilo enlazados por puentes metilénicos. Las ciclodextrinas han demostrado utilidad en la encapsulación de fármacos como la camptotecina (6). En la Figura 1 se muestran distintos ejemplos de cavitandos de ciclodextrinas asociados a polímeros, formando nanoesponjas así como a otros materiales nanoestructurados, como es el caso de los nanotubos de carbono (7). En analogía con los éteres corona, los azacriptandos son cavitandos especialmente útiles para el reconocimiento de aniones (8).
Figura 1. Encapsulación de fármacos por ciclodextrinas (CDs). Polímeros CDs formando nanoesponjas. Simbiosis de materiales nanoestructurados y CDs. PEG: polietilenglicol. CNT: nanotubos de carbono. SW-CNT: nanotubos de carbono de pared recubierta.
Uno de los retos a día de hoy es la discriminación quiral, ya que los enantiómeros poseen idénticas propiedades físicas y físico químicas pero difieren en su reactividad y en su interacción con entidades biológicas quirales, como las proteínas (un ejemplo: el R- y el S-limoneno presentes, respectivamente, en la naranja y el limón condicionan distintos aromas). Una de las aplicaciones más relevantes de los cavitandos es el reconocimiento quiral de los compuestos orgánicos debido a que la disposición espacial de las moléculas conlleva diferente afinidad por las “host molecules”. Así, las ciclodextrinas han encontrado una gran utilidad como componentes de las fases estacionarias o de las fases móviles en las distintas técnicas analíticas de separación (cromatografía -de líquidos, de gases, de fluidos supercríticos- y electroforesis capilar) (9,10). Así mismo, algunos derivados de calixareno se han utilizado con éxito para la discriminación quiral de los enantiómeros del ácido mandélico (11).
3. CICLODEXTRINAS
Las ciclodextrinas (CDs) ofrecen numerosas ventajas comparadas con otros cavitandos, ya que son productos naturales, se obtienen a partir del almidón, lo cual las hace muy atractivas desde el punto de vista de la química sostenible. Se producen a escala industrial a través de un proceso enzimático relativamente sencillo y a un precio razonable. Los efectos secundarios o tóxicos que pueden manifestarse son prácticamente inexistentes por lo que se utilizan en la industria farmacéutica, cosmética y alimentaria. Son capaces de encapsular, aislar y compartimentalizar una gran variedad de compuestos, ya que existen diversos tamaños fácilmente acomodables a los requerimientos de los compuestos a incluir. (12-14). Todo ello las hace atractivas en muy distintos campos de la ciencia desde la tecnología farmacéutica, o la química, a la nanotecnología.
4. CICLODEXTRINAS EN TECNOLOGÍA FARMACÉUTICA
Uno de los aspectos más representativos del uso de ciclodextrinas en la industria, es su aplicación en tecnología farmacéutica para mejorar la solubilidad y estabilidad de fármacos, lo cual directamente repercute en una mejora de la eficacia de los mismos a través de incremento de la biodisponibilidad por ser capaces de trasladar sin alteraciones a los fármacos a su lugar de acción, ello conlleva un incremento en las concentraciones plasmáticas de los principios activos (4,15,16). La monografía correspondiente a la 𝛽-CD forma parte de Farmacopeas como la Europea, la de Estados Unidos o la de Japón. En las Tablas 1 y 2 se muestra, a modo de ejemplo, algunos de los principios activos que se formulan con diversas CDs para mejorar sus propiedades tecnológicas y biofarmacéuticas. Muchos principios activos ven reducida su efectividad farmacológica como consecuencia de pobre estabilidad química o fotoquímica (17). La inclusión en las cavidades de las ciclodextrinas aísla unas moléculas de otras y las individualiza, impidiendo de este modo determinadas reacciones indeseadas y logrando una mejora en la estabilidad de los principios activos.
Tabla 1: Principios activos formulados con ciclodextrinas y recogidos en varias farmacopeas.
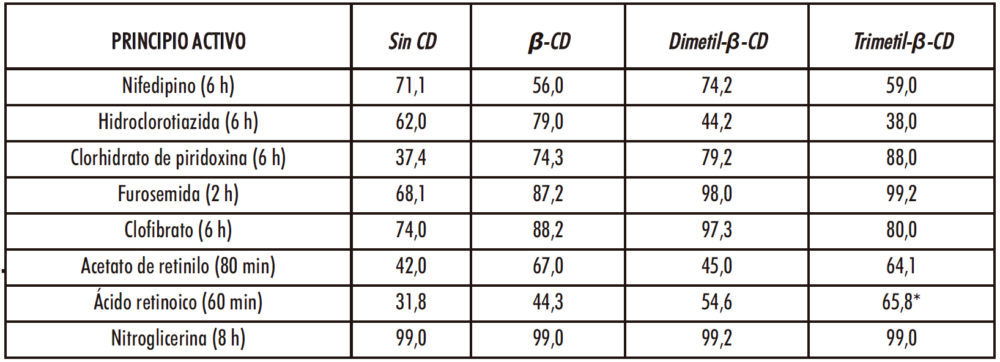
Tabla 2 : Mejora en la estabilidad de fármacos como consecuencia de la inclusión en las cavidades de ciclodextrinas (CDs). Se muestra el porcentaje de principio activo no alterado después de el tiempo de irradiación (entre paréntesis). Comparación de los porcentajes de los principios activos incluidos en CDs con relación al fármaco libre.
*Corresponde a 2-hidroxipropil-β-CD en lugar de a trimetil β-CD
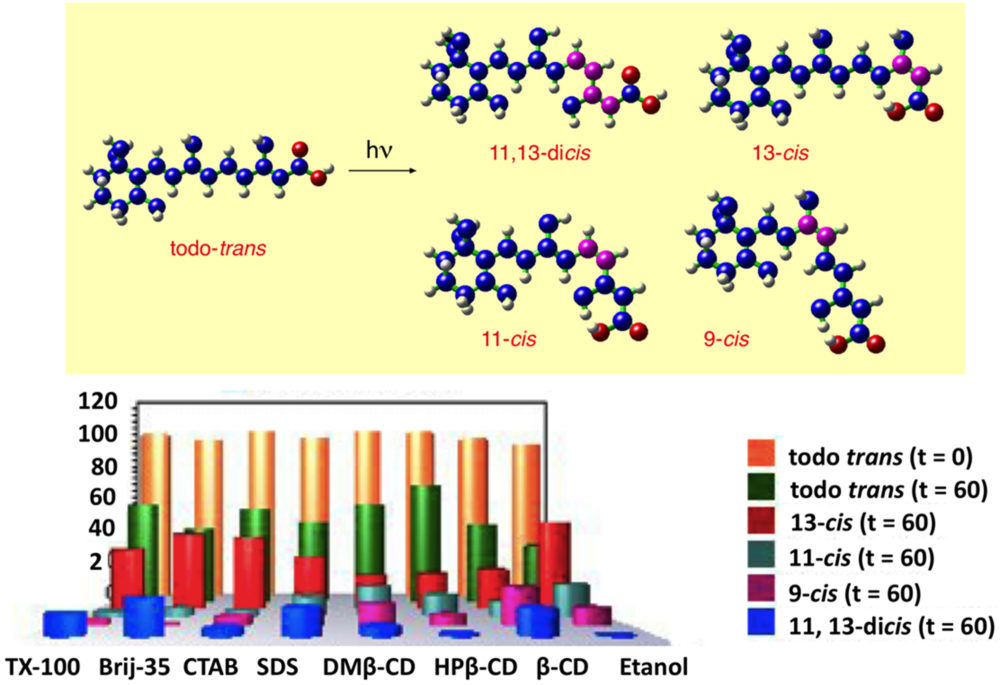
Este es el caso de los retinoides, compuestos susceptibles de isomerización por vía fotoquímica. Nuestro grupo ha demostrado que, tanto en el caso del retinal como del ácido retinoico, se produce un efecto muy beneficioso en la estabilización de las formas con actividad biológica, los isómeros todo-trans. Los derivados todo-trans ven muy dificultada la isomerización por vía radiante, cuando son incluidos en 𝛽-CD y sus derivados 2-hidroxipropil-𝛽-CD (HP𝛽-CD), 2,3 di-O-metil-𝛽-CD (DM𝛽-CD) y 2,3,6-tri-O-metil-𝛽-CD (TM𝛽-CD). Así mientras que tras 60 minutos de irradiación en etanol del todo-trans ácido retinoico se transforma en los diferentes cis- derivados quedando solo un 31 % de forma activa, para el ácido retinoico incluido la HP𝛽-CD permanece como forma todo-trans con un porcentaje del 68% (Figura 2). Todas las ciclodextrinas estudiadas aportan una significativa protección, de tal modo que la irradiación no llega a transformar ni tan siquiera un 50% del isómero todo-trans (18).
Figura 2. Estabilización de fármacos mediante nanoencapsulación en CDs. Variación de la proporción del ácido todo trans-retinoico antes y después de la isomerización por vía fotoquímica. Porcentaje de los isómeros del ácido retinoico producidos tras 60 minutos de irradiación en diferentes entornos: etanol, tensioactivos (Triton X-100, Brij-35, CTAB y SDS) y ciclodextrinas. La cuantificación se llevó a cabo por HPLC-UV (18).
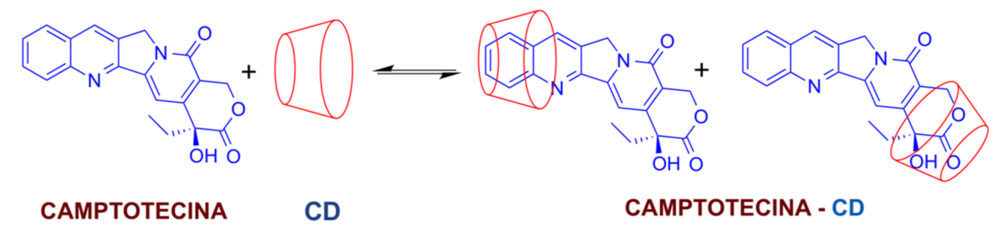
La ciclodextrinas presentan una buena hidrosolubilidad gracias a los grupos hidrófilos de su parte exterior; sin embargo, el interior de la cavidad es hidrofóbico permitiendo de este modo alojar fármacos que poseen una escasa solubilidad en agua. Por ello, la inclusión de fármacos que experimenten un incremento es su solubilidad conlleva mejor distribución y biodisponibilidad los principios activos. En este sentido, además se dispone de ciclodextrinas químicamente modificadas con grupos metilo e hidroxipropilo que contribuyen a incrementar la hidrosolubilidad con respecto a las CDs naturales, y en este aspecto, el grado de sustitución juega un importante papel en el incremento de la hidrosolubilidad así como en el aumento de tamaño de la cavidad de las CDs (19). Entre los ejemplos de mejora de la solubilidad comentaremos nuestra propia experiencia con la mejora en las solubilización de los antitumorales inhibidores de topoisomerasas, camptotecina y luotonina A. Ambos experimentan un considerable incremento en la solubilidad en agua en presencia de 𝛽-CD y de HP𝛽-CD. Uno de los derivados de luotonina A, mas hidrofóbico debido a la naturaleza de los sustituyentes, tiene una mejora aun mayor en la solubilidad. La metodología desarrollada para estos ensayos de solubilidad están de acuerdo con los principios establecidos de la Química Sostenible y además se confirmó por espectrometría de masas que los complejos mayoritarios son de estequiometría 1:1 (Figura 3) tanto en el caso de la CPT como de la luotonina A (20).
Figura 3. Complejos de inclusión del antitumoral camptotecina y 𝛽-CD modificadas (20).
5. CICLODEXTRINAS Y PRETRATAMIENTO ANALÍTICO
La etapa de pre-tratamiento de las muestras, a día de hoy sigue siendo la más laboriosa y la de mayor dificultad en cuanto a automatización y a reproducibilidad. La elección de un procedimiento de preparación y tratamiento de las muestras es determinante para que el resultado del análisis sea fiable (21-23).
Los materiales que integran soporte extractante para retener los analitos pueden agruparse en tres grandes grupos:
a) Materiales nanoestructurados, incluyendo nanotubos de carbono y nanopartículas magnéticas.
b) Materiales adsorbentes basados en el reconocimiento molecular, entre los que sobresalen los polímeros impresos e inmuno-sorbentes.
c) Redes metal-compuesto orgánico, un tipo de material híbrido constituido por elementos orgánicos e inorgánico de elevada porosidad y polaridad ajustable (24).
Gracias al reconocimiento molecular altamente selectivo de las cavidades de las ciclodextrinas hacia muy diversos analitos, estos cavitandos se han empleado con éxito a través de la funcionalización de la superficie adsorbente con CDs de tal manera que estas retengan ciertos compuestos separándolos del resto de los componentes de la muestra.
Entre las distintas metodologías analíticas destinadas a la pre-concentración, limpieza y purificación de analitos sobresale por su eficacia y robustez la extracción en fase sólida (SPE). En la década de los años noventa se desarrollan las técnicas de microextracción en fase sólida (SPME) con el principal objetivo de reducir el consumo de tiempo y de disolventes pero manteniendo la eficacia de extracción (25). Aunque las configuraciones y disposición de los materiales extractantes en ambas metodologías analíticas son muy variadas, quedando fuera de este contexto por su extensión; sin embargo, si nos detendremos en algunos aspectos generales comunes a ambas metodologías.
5.1. Purificación y extracción mediante el empleo de polímeros de ciclodextrinas
Estas metodologías se basan en la preparación de nano-esponjas constituidas por CDs y diseñadas con la finalidad de retener compuestos o analitos. La polimerización de las CDs es uno de los primeros recursos para la extracción eficaz de múltiples analitos. La eficacia de la extracción es función de la estabilidad de los complejos formados así como de la capacidad de carga de los materiales soporte utilizados.
Se denominan nano-esponjas (Figura 1) a una nueva clase de polímeros con un elevado número de enlaces entrecruzados (“hyper cross-linked”) constituidos a partir de estructuras coloidales que alojan en su interior cavitandos con cavidades de unos pocos nanómetros de diámetro interno (26,27). Las ciclodextrinas son unos de los cavitandos utilizados con gran éxito en la síntesis de nano-esponjas por su eficacia en la extracción de numerosos analitos y en la vehiculización de fármacos (28).
5.2 Purificación y extracción mediante materiales nanoestructurados que implican ciclodextrinas
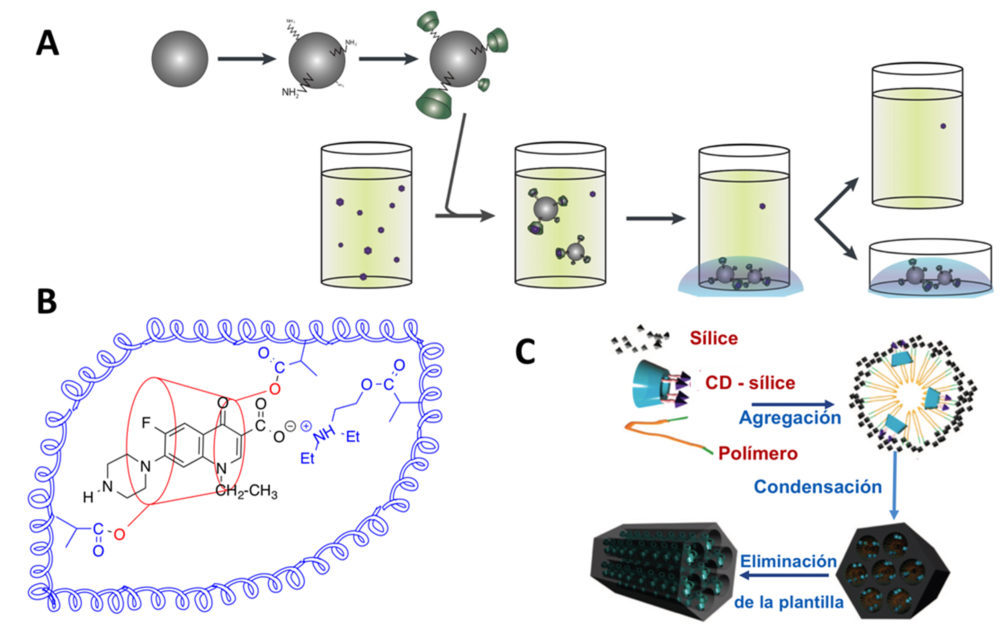
Un procedimiento muy utilizado por la sencillez es el empleo de partículas magnéticas. Estas partículas de oxido férrico pueden funcionalizarse mediante un tratamiento adecuado (propiletilsiloxano) quedando de este modo un núcleo denso de magnetita recubierto por una superficie de sílice funcionalizada con grupos amino a los que en el siguiente paso de la síntesis se enlazarán las ciclodextrinas. La partículas funcionalizadas y recubiertas con CDs se suspenden en el medio acuoso al que se añade la muestra biológica a analizar (sangre, plasma, orina…), de este modo, solo aquellos analitos que se adapten por su tamaño y polaridad se incluirán en la CDs. Transcurrido el tiempo necesario se aplica un campo magnético de tal manera que todas las partículas magnéticas, junto con los analitos extraídos, van al fondo del vaso de precipitados, pudiéndose separar fácilmente del resto de la muestra. (Figura 4A).
Figura 4. CDs como base para sistemas de pretratamiento analítico de muestras. (A) Nanopartículas magnéticas modificadas con CDs para la eficaz y selectiva extracción de analitos en muestras biológicas; (B) polímeros impresos utilizando CDs para la extracción selectiva de antibióticos (quinolonas); (C) polímeros impresos utilizando CDs y otros materiales nanoestructurados de elevada capacidad de extracción.
El empleo de nanopartículas magnéticas presenta diversas ventajas comparado con los métodos tradicionales de extracción, así, la síntesis y funcionalización de las partículas magnéticas es relativamente asequible. La magnetita y los óxidos de hierro empleados en la obtención del núcleo central es económico y está disponible comercialmente y el material poroso (sílice) que en numerosas ocasiones se emplea para recubrir las partículas magnéticas es igualmente económico. La separación de las partículas magnéticas que han atrapado los principios activos es sencilla, y no requiere instrumentación, simplemente aplicar un campo magnético para a atraer a las partículas al fondo, por lo que la separación es rápida y eficaz. Por otra parte la eficacia de extracción de los compuestos diana por parte de las ciclodextrinas el alta, obteniendo una elevada eficacia de extracción.
Este procedimiento se ha empleado con éxito para la extracción de benzodiacepinas de muestras de sangre (29) y de ácido 5-hidroxi-3-indolacético como biomarcador tumoral en muestras de orina (30).
5.3 Purificación y extracción mediante polímeros impresos
La idea de atrapar compuestos en una matriz complementaria y vacía fue propuesta por Wulff and Sarhan en 1972, sin embargo no es hasta la década de los años noventa cuando Sellergren describe el potencial de estos materiales como adsorbentes para SPE y comienza su utilización mediante la síntesis de materiales adsorbentes basados en esta idea (31, 32). Si pensamos que en un fósil podemos identificar una especie vegetal, porque solo ella es capaz de dejar esa huella, tenemos un buen símil para imaginar la buena selectividad de este tipo de materiales destinados al reconocimiento molecular de analitos específicos. Teniendo como plantilla el compuesto diana a analizar, este se unirá por interacciones no covalentes (dipolo-dipolo, enlaces de hidrógeno, interacciones electrostáticas,…) a un mínimo de tres monómeros funcionales capaces de reconocer molecularmente puntos clave en el compuesto diana. Tras un proceso de polimerización en el que se forman enlaces entrecruzados se obtiene una matriz adsorbente sólida de la que con un procedimiento de lavado adecuado, extraeremos el compuesto diana que ha actuado como plantilla. De este modo queda libre el polímero impreso y disponible para reconocer y atrapar las moléculas de analito análogas a la plantilla y presentes en las muestras problema.
Los polímeros impresos presentan ventajas frente a otros materiales adsorbentes como son su selectividad y su robustez acompañadas de una elevada estabilidad química y térmica. Estas características no las poseen los adsorbentes basados en proteínas, anticuerpos y ácidos nucleicos, que si bien presentan una elevada selectividad, sin embargo son bastante lábiles (33).
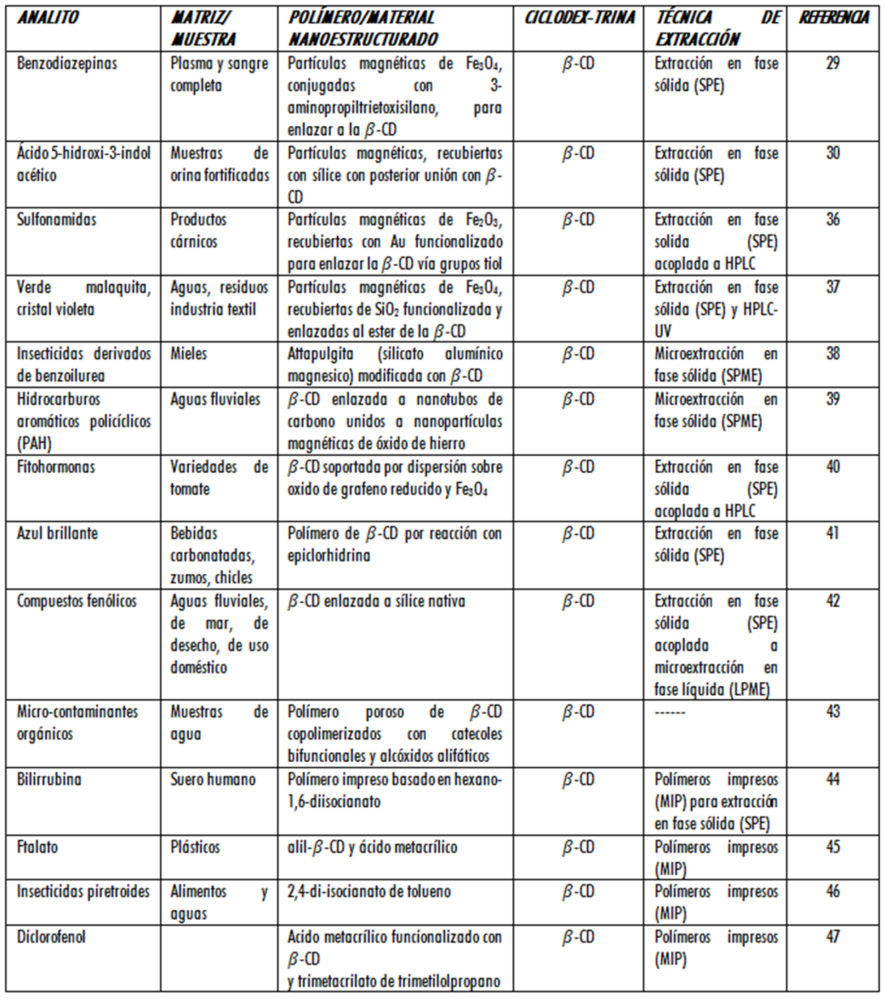
En la Figura 4B se presenta un polímero impreso que emplea 𝛽-CD para la extracción antibióticos derivados de fluoroquinolona (norfloxacino) de muestras de agua (34). Los polímeros impresos que involucran a ciclodextrinas como parte esencial de la plantilla extractante poseen una elevada selectividad y un alto rendimiento de extracción comparados con otros materiales y se han empleado con éxito en la extracción de fármacos, plaguicidas, hormonas y aditivos de plásticos entre otros ejemplos (35). En la Tabla 3, se recoge un resumen de ejemplos de extracciones en fase sólida y micro-extracciones en fase sólida, en los que se utilizan materiales adsorbentes con CDs, bien sea, en la modalidad de partículas magnéticas, de materiales nano-estructurados o de polímeros impresos.
Tabla 3: Ejemplos de empleo de polímeros y materiales nanoestructurados que utilizan ciclodextrinas para el pre-tratamiento analítico de muestras.
6. CICLODEXTRINAS EN SEPARACIONES CROMATOGRÁFICAS
Las posibilidades de sustitución química de los hidroxilos primarios y secundarios de las ciclodextrinas así como la de emplear como cavitandos de partida los derivados naturales a- β- y 𝛾-ciclodextrina, proporcionan una alta capacidad de reconocimiento molecular notablemente selectivo y acomodable o modificable en función de las características de los analitos a separar (48).
La sustitución con diferentes grupos funcionales, ya sea polares como de baja polaridad, permite establecer múltiples interacciones intermoleculares de tipo electrostático, pares iónicos, dipolo-dipolo, puentes de hidrógeno o apilamiento 𝜋- 𝜋 (49).
6.1 Ciclodextrinas en separaciones quirales
Las separaciones cromatográficas quirales constituyen uno de los retos de la cromatografía analítica con el objetivo de la resolución de mezclas quirales en la industria farmacéutica, biotecnológica y alimentaria. Las separaciones quirales por cromatografía de líquidos se han incrementado exponencialmente gracias a su robustez como técnica de análisis y a la gran aplicación en análisis cuantitativo. Asimismo, se emplean con gran éxito en separaciones preparativas a gran escala y a escala intermedia en la industria. La inmovilización de distintos derivados de ciclodextrina sobre la superficie de las partículas de sílice (50) a través de enlaces tipo éter, urea o amino da lugar a fases estacionarias quirales (Figura 5) que presentan muy alta enantioselectividad y adecuada estabilidad química (51,52).
Figura 5. Fases estacionarias quirales (CSP) para la separación de analitos por cromatografía de líquidos (HPLC). (A) Reacciones de modificación de la superficie de la sílice incorporando CDs en su superficie. (B) Esquema de retención de analitos por ciclodextrinas en el interior de una columna cromatográfica quiral. (C) Partículas de sílice incorporando ciclodextrinas químicamente modificadas para incrementar la enantioselectividad de la separación. (D) Cromatograma mostrando la resolución quiral de flavanonas R: Respuesta del detector; tR: tiempo de retención (49, 52).
Una alternativa a las fases estacionarias quirales, muy empleada y de gran utilidad es la utilización de fases estacionarias no quirales, es decir fases estacionarias convencionales análogas a las utilizadas en las separaciones rutinarias, combinadas con fases móviles que incorporan ciclodextrinas como aditivos en las fases móviles para lograr la discriminación quiral. En esta modalidad de separación quiral se emplean tanto las ciclodextrinas naturales como las químicamente modificadas. Así la sulfobutiléter-β-ciclodextrina, en la que están sustituidos los OH de las posiciones 2, 3 y 6, conocida con el nombre comercial de captisol®, se emplea ampliamente en la industria farmacéutica para la purificación de analitos quirales, pero también se han empleado en la separación de péptidos y proteínas (53). La 2-hidroxipropil-β-ciclodextrina proporciona muy buena enantio-resolución en el caso de las denominadas “drogas de diseño” como es el caso de los derivados de fenetilaminas y catinonas con estructura de β-ceto-fenetilaminas (54).
El efecto de la β-ciclodextrina nativa y de la dimetil- β-ciclodextrina, permite la separación quiral de una treintena de compuestos, sin embargo la mejor resolución se consigue en presencia de 2-hidroxipropil-β-ciclodextrina en concentración 20 mM en la fase móvil. Los resultados se comparan con los obtenidos en análogas condiciones en separación por electroforesis capilar. La influencia de la naturaleza química y de la concentración de ciclodextrina también es clave para lograr los objetivos de separación quiral en 10 derivados de ácido mandélico (55).
6.2 Ciclodextrinas en separaciones químicamente sostenibles
La cromatografía de líquidos es una técnica robusta ampliamente utilizada en la industria, y en la que un equipo de HPLC genera alrededor de 500 mL diarios de residuos potencialmente dañinos para el medio ambiente. En los últimos 20 años ha crecido el interés por buscar metodologías analíticas sostenibles, entre ellas el empleo de disolventes respetuosos con el medio ambiente constituyen una tendencia creciente (56, 57). El empleo de ciclodextrinas como aditivos en las fases móviles en cromatografía permite reducir la proporción de disolvente orgánico en la fase móvil a la vez que incrementa la eficacia y la resolución. La combinación de una fase estacionaria de tipo metilsilano (C1) con etanol y ciclodextrinas en la fase móvil permite reducir entre un 50 y un 70 % la proporción de disolvente orgánico en la fase móvil con respecto a otras metodologías de separación que no emplean ciclodextrinas en las fases móviles (Figura 6) (58).
Figura 6. Ciclodextrinas como modificadores de las fases móviles en cromatografía de líquidos (HPLC). (A) Equilibrios de distribución en presencia de CDs (B) Cromatograma mostrando la mejora en la eficacia de las separaciones en presencia de 2-hidroxipropil-𝛽-CD. R: Respuesta del detector; tR: tiempo de retención; IS: patrón interno; 1: norharmano; 2: harmano; 3: harmina. (C) Reducción de la proporción de disolventes orgánicos en las fases móviles que incorporan ciclodextrinas. Volumen de disolvente orgánico consumido en la separación cromatográfíca según el procedimiento de separación (58).
La introducción de ciclodextrinas como modificadores en las fases móviles (mobile phase additives, MPA) supone la introducción de un equilibrio secundario al equilibrio principal en cromatografía, esto es el equilibrio de distribución de los analitos entre la fase estacionaria y la fase móvil. La inclusión de los analitos en las cavidades de las ciclodextrinas, provoca una importante disminución en los tiempos de retención (59) y en los factores de retención de los analitos y ello se debe al aumento de la solubilidad de los analitos en las fases móviles y además se incrementa la resolución y la eficacia de la separación y con significativas ventajas desde el punto de vista de la sostenibilidad (60).
7. CICLODEXTRINAS EN LA RECUPERACIÓN DEL MEDIO AMBIENTE
El 23 de mayo de 2001, 179 países ratificaron los acuerdos que se denominan “Acuerdos de Estocolmo”. En el se comprometen a la eliminación paulatina de los denominados “contaminantes orgánicos persistentes” (POPs, persistent organic pollutants), estos acuerdos entraron en vigor en 2004 y ello ha motivado un interés creciente en la búsqueda de vías de eliminación respetuosas con el medio ambiente para todo este tipo de compuestos. En este sentido la síntesis de polímeros adsorbentes basados en ciclodextrinas para la captura de distintos materiales presentes en el medioambiente, resulta muy atractiva y además notoriamente exitosa (61). La elevada superficie específica así como la notable porosidad de los polímeros basados en ciclodextrinas hacen de estos, unos materiales adsorbentes extremadamente útiles en la recuperación y el tratamiento de aguas y de suelos con el fin de evitar la presencia de residuos nocivos en los mismos (62). Por ello se utilizan con gran éxito en plantas de purificación agua (63) para la captación de una gran variedad de contaminantes como medicamentos (64, 65), colorantes (66, 67) y contaminantes volátiles persistentes (68, 69). Igualmente se ha descrito su utilización en la captación de metales pesados (70, 71). Se han puesto en marcha distintas metodologías para la destrucción y eliminación de los elementos contaminantes presentes en el medioambiente, entre las más exitosas y eficaces sobresalen las técnicas de oxidación y de foto-catálisis; sin embargo, las metodologías basadas en procesos de adsorción son muy ventajosas por su bajo costo, facilidad de operación y elevada eficacia. Es en este escenario de las metodologías de adsorción donde las ciclodextrinas, sus polímeros, nano-esponjas y asociaciones de estas con otros materiales adsorbentes (nanotubos de carbono y sílice) son sumamente atractivas y con un futuro prometedor.
8. CONCLUSIONES
Se ha revisado el papel de las ciclodextrinas en distintos aspectos como la tecnología farmacéutica, la química analítica, ya sea en la etapa pre-analítica o bien en la etapa analítica propiamente dicha, y mas, concretamente en las determinaciones por cromatrografía. El papel de las ciclodextrinas como elementos adsorbentes esenciales para la recuperación del medioambiente captando los compuestos responsables de las contaminación ambiental es especialmente significativo. Se ha centrado el enfoque en las aplicaciones analíticas de las ciclodextrinas por ser objeto de nuestros trabajos de investigación desde hace casi 30 años. Su singularidad como cavitandos altamente selectivos capaces de captar y discriminar compuestos quirales, y diferenciar entre análogos químicamente y estructuralmente relacionados les confiere propiedades y aplicaciones únicas. A ello que hay que unir su relativa facilidad de producción a partir de fuentes naturales y siendo totalmente sostenibles por tratarse de compuestos naturales.
Agradecimientos
Mi reconocimiento y gratitud a los Excelentísimos Sres. Académicos D. Benito del Castillo, D. Bartolomé Ribas y D. José Carlos Menéndez y muy especialmente al Excelentísimo. Sr. Académico D. Fidel Ortega por su disponibilidad y su generosidad al haber aceptado mi presentación. A todos mis compañeros y colaboradores en los diferentes proyectos de investigación. Al Ministerio de Ciencia e Innovación; y a la Universidad Complutense de Madrid, la financiación.
9. REFERENCIAS
- Shenderovich, IG. Gulliver in the country of Lilliput: an interplay of noncovalent interactions. Molecules 2021; 26: 158-161.
- Ariga K, Kunitake T. Supramolecular Chemistry. Fundamentals and Applications, Berlín Heidelberg: Springer-Verlag 2006.
- Schneider, HJ. Binding mechanisms in supramolecular complexes. Angew Chem Int Ed 2009; 48: 3924 – 3977.
- Davis ME, Brewster ME. Cyclodextrin-based pharmaceutics: past, present and future. Nat Rev Drug Discov 2004; 3: 1023-1035.
- Lagona J, Mukhopadhyay P, Chakrabarti S, Isaacs, L. The cucurbit (n) uril family. Angew Chem Int Ed 2005; 44: 4844-4870.
- Gavvala K, Sengupta A, Hazra P. Modulation of photophysics and pKa shift of the anticancer drug camptothecin in the nanocavities of supramolecular hosts. ChemPhysChem 2013; 14: 532 – 542.
- Li J. Cyclodextrin inclusion polymers forming hydrogels. Adv Polym Sci 2009; 175-203.
- Kang SO, Llinares, JM, Dayc VW, Bowman-James K. Cryptand-like anion receptors. Chem Soc Rev 2010; 39: 3980 – 4003.
- Anderson J, Berthod A, Pino V, Stalcup AM. Analytical Separation Science, volumen 5, Wiley-VCH, 2016.
- Szabo ZI, Foroughbakhshfasaei M, Gal R, Horwátz P, Komjati B, Noszál B, Tóth G. Chiral separation of lenalidomide by liquid chromatography on polysaccharide-type stationary phases and by capillary electrophoresis using cyclodextrin selectors. J Sep Sci 2018; 41: 1414-1423.
- Zhengyi L, Kun Z, Yuan L, Xiaoqiang S, Leyong W. Synthesis of calix(4)proline derivatives and their chiral recognition for enantiomers of mandelic acid. Chin J Org Chem 2015; 35: 1531-1536.
- Crini G. Review: A History of Cyclodextrins. Chem Rev 2014; 114: 10940-10975.
- Dodziuk H. (Ed.), Cyclodextrins and their Complexes, Wiley-VCH, 2006.
- Bilensoy E. (Ed.), Cyclodextrins in Pharmaceutics, Cosmetics, and Biomedicine, John Wiley & Sons, 2011.
- Kurkov SV, Loftsson T. Cyclodextrins. Int J Pharmaceut 2013; 453: 167 – 180.
- Uekama K, Hirayama F. Improvement of drug properties by cyclodextrins, pags. 813-840. In: The practice of medicinal chemistry, Academic Press, 2008.
- Popielec A, Loftsson T. Effects of cyclodextrins on the chemical stability of drugs. Int J Pharmaceut 2017; 531: 532 – 542.
- Muñoz-Botella S, Martín MA, del Castillo B, Lerner DA, Menéndez JC. Differentiating geometrical isomers of retinoids and controlling their photo-isomerization by complexation with cyclodextrins. Anal Chim Acta 2002; 468: 161-170.
- Saokham P, Muankaew C. Jansook P, Loftsson T. Solubility of cyclodextrins and drug/cyclodextrin complexes. Molecules 2018; 23: 1161 – 1175.
- González-Ruiz V, Olives AI, Martín MA. A down-scaled fluorimetric determination of the solubility properties of drugs to minimize waste generation. Green Chem 2013; 15: 2558 – 2565.
- Buszewski B, Szultka M. Past, present, and future of solid phase extraction: a review. Crit Rev Anal Chem 2012; 42: 198 – 213.
- Andrade-Eiroa A, Canle M, Leroy-Cancellieri V, Cerdá V. Solid-phase extraction of organic compounds: A critical review (Part I). Trend Anal Chem 2016; 80: 641 – 654.
- Andrade-Eiroa A, Canle M, Leroy-Cancellieri V, Cerdá, V. Solid-phase extraction of organic compounds: A critical review. (Part II). Trend Anal Chem 2016; 80: 655 – 667.
- Płotka-Wasylka J, Szczepańska N, de la Guardia M, Namieśnik J. Modern trends in solid phase extraction: new sorbent media. Trend Anal Chem 2016; 77: 23 – 43.
- Mehdinia A, Aziz-Zanjani MO. Advances for sensitive, rapid and selective extraction in different configurations of solid-phase microextraction. Trend Anal Chem 2013; 51: 13 – 22.
- Trotta F, Zanetti M, Cavalli R. Cyclodextrin-based nanosponges as drug carriers. Beilstein J Org Chem 2012; 8: 2091-2099.
- Swaminathan S, Pastero L, Serpe L, Trotta F, Vavia P, Aquilano D, Trotta M, Zara GP, Cavalli, R. Cyclodextrin-based nanosponges encapsulating camptothecin: physicochemical characterization, stability and cytotoxicity. Eur J Pharm Biopharm 2010; 74: 193-201.
- Sherje AP, Dravyakar BR, Kadam D, Jadhav M. Cyclodextrin-based nanosponges: A critical review. Carbohyd Polym 2017; 173: 37 – 49.
- Cai K, Li J, Luo Z, Hu Y, Hou Y, Ding X. β-Cyclodextrin conjugated magnetic nanoparticles for diazepam removal from blood. Chem Commun 2011; 47: 7719 – 7721.
- Gaber-Ahmed GH, Badía-Laíño R, García-Calzón JA, Díaz-García ME. Magnetic nanoparticles grafted with β-cyclodextrin for solid-phase extraction of 5-hydroxy-3-indole acetic acid. Microchim Acta 2014; 181: 941 – 948.
- Buszewski B, Szultka M. Past, Present, and Future of Solid Phase Extraction: A Review. Crit Rev Anal Chem 2012; 42: 198 – 213.
- Azzouz A, Kailasa SK, Lee SS, Rascón AJ, Ballesteros E, Zhang M, Kim KH. Review of nanomaterials as sorbents in solid-phase extraction for environmental samples. Trend Anal Chem 2018; 108: 347- 369.
- Płotka-Wasylka J, Szczepańska N, de la Guardia M, Namieśnik J. Modern trends in solid phase extraction: New sorbent media. Trend Anal Chem 2016; 77: 23 – 43.
- Xua Z, Kuang D, Liu L, Dengb Q. Selective adsorption of norfloxacin in aqueous media by an imprinted polymer based on hydrophobic and electrostatic interactions. J Pharm Biomed Anal 2007; 45: 54–61.
- Lay S, Ni X, Yu H, Shen S. State-of-the-art applications of cyclodextrins as functional monomers in molecular imprinting techniques: a review. J Sep Sci 2016; 39: 2321 – 2331.
- Yang Y, Li G, Wu D, Wen A, Wu Y, Zhou X. β-Cyclodextrin-/AuNPs-functionalized covalent organic framework-based magnetic sorbent for solid phase extraction and determination of sulfonamides. Microchim Acta 2020; 187: 278 -288.
- Shahrebabak SM, Saber-Tehrani M, Faraji M, Shabanian M, Aberoomand-Azar P. Magnetic solid phase extraction based on poly(β-cyclodextrin-ester) functionalized silica-coated magnetic nanoparticles (NPs) for simultaneous extraction of the malachite green and crystal violet from aqueous samples. Environ Monit Assess 2020; 192; 262-275.
- Zhang P, Cui X, Yang X, Zhang S, Zhou W, Gao H, Lu R. Dispersive micro-solid-phase extraction of benzoylurea insecticides in honey samples with a β-cyclodextrin-modified attapulgite composite as sorbent. J Sep Sci 2016; 39: 412 – 418.
- Yazdanpanah M, Nojavan S. Micro-solid phase extraction of some polycyclic aromatic hydrocarbons from environmental water samples using magnetic β-cyclodextrin-carbon nano-tube composite as a sorbent. J Chromatogr A 2019; 1585: 34 – 45.
- Li N, Chena J, Shi YP. Magnetic reduced graphene oxide functionalized with β-cyclodextrins magnetic solid-phase extraction adsorbents for the determination of phytohormones in tomatoes coupled with high performance liquid chromatography. J Chromatogr A 2016; 1441: 24 – 33.
- Li R, Jiang ZT, Wang RX. Solid Phase Extraction Combined Direct Spectrophotometric Determination of Brilliant Blue in Food Using β-Cyclodextrin Polymer. Food Anal Methods 2009; 2: 264 – 270.
- Faraji H, Husain SW, Helalizadeh M. Determination of phenolic compounds in environmental water samples after solid phase extraction with β-cyclodextrin-bonded silica particles coupled with a novel liquid-phase microextraction followed by gas chromatography-mass spectrometry J Sep Sci 2012; 35: 107 – 113.
- Alsbaiee A, Smith BJ, Xiao L, Ling Y, Helbling DE, Dichtel WR. Rapid removal of organic micropollutants from water by a porous β-cyclodextrin polymer. Nature 2016; 529: 190 – 194.
- Yang Y, Long Y, Cao Q, Li K, Liu F. Molecularly imprinted polymer using β-cyclodextrin as functional monomer for the efficient recognition of bilirubin. Anal Chim Acta 2008; 606: 92 – 97.
- Yongfeng K, Wuping D, Yan L, Junxia K, Jing X. Molecularly imprinted polymers of allyl-β-cyclodextrin and methacrylic acid for the solid-phase extraction of phthalate. Carbohyd Polym 2012; 88: 459 – 464.
- Guo Y, Liang X, Wang Y, Liu Y, Zhu G, Gui W. Cyclodextrin-based molecularly imprinted polymers for the efficient recognition of pyrethroids in aqueous media. J Appl Polym Sci 2013; 128: 4014 – 4022.
- Surikumaran H, Mohamad S, Sarih NM. Molecular imprinted polymer of methacrylic acid functionalised β-cyclodextrin for selective removal of 2,4-dichlorophenol. Int J Mol Sci 2014; 15: 6111 – 6136.
- Ikai T, Okamoto Y. Structure control of polysaccharide derivatives for efficient separation of enantiomers by chromatography. Chem Rev 2009; 109: 6077 – 6101.
- Zhou J, Yang B, Tang J, Tang W. Cationic cyclodextrin clicked chiral stationary phase for versatile enantioseparations in high-performance liquid chromatography. J Chromatogr A 2016; 1467: 169 – 177.
- Silva M, Pérez-Quintanilla D, Morante-Zarcero S, Sierra I, Marina ML, Aturki Z, Fanali S. Ordered mesoporous silica functionalized with β-cyclodextrin derivative for stereoisomer separation of flavanones and flavanone glycosides by nano-liquid chromatography and capillary electrochromatography. J Chromatogr A 2017; 1490: 166 – 176.
- Yao X, Tan TTY, Wang Y. Thiol–ene click chemistry derived cationic cyclodextrin chiral stationary phase and its enhanced separation performance in liquid chromatography. J Chromatogr A 2014; 1326: 80 – 88.
- Pang L, Zhou J, Tang J, Ng SC, Tang W. Evaluation of perphenylcarbamated cyclodextrin clicked chiral stationary phase for enantioseparations in reversed phase high performance liquid chromatography. J Chromatogr A 2014; 1363: 119 – 127.
- Kučerová G, Procházková H, Kalíkova K, Tesařová E. Sulfobutylether-β-cyclodextrin as a chiral selector for separation of amino acids and dipeptides in chromatography. J Chromatogr A 2016; 1467: 356 – 362.
- Li L, Lurie IS. Regioisomeric and enantiomeric analyses of 24 designer cathinones and phenethylamines using ultra high performance liquid chromatography and capillary electrophoresis with added cyclodextrins. Foresnic Sci Int 2015; 254: 148-157.
- Tong S, Zhang H, Shen M, Ito Y, Yan J. Enantioseparation of mandelic acid derivatives by high performance liquid chromatography with substituted β-cyclodextrin as chiral mobile phase additive and evaluation of inclusion complex formation. J Chromatogr B 2014; 962: 44 – 51.
- Olives AI, González-Ruiz V, Martín MA. Sustainable and Eco-Friendly Alternatives for Liquid Chromatographic Analysis. ACS Sustain Chem Eng 2017; 5: 5618−5634.
- Dembek M, Bocian S. Pure water as a mobile phase in liquid chromatography techniques. Trend Anal Chem 2020; 123: 115793
- González-Ruiz V, Olives AI, Martín MA. SPE/RP-HPLC using C1 columns: an environmentally friendly alternative to conventional reverse-phase separations for quantitation of beta-carboline alkaloids in human serum samples. Anal Bioanal Chem 2011; 400: 395 – 401.
- León AG, Olives AI, del Castillo B, Martín MA. Influence of the presence of methyl cyclodextrins in high-performance liquid chromatography mobile phases on the separation of β-carboline alkaloids. J Chromatogr A 2008; 1192: 254 – 258.
- González-Ruiz V, León AG, Olives AI, Martín MA, Menéndez JC. Eco-friendly liquid chromatographic separations based on the use of cyclodextrins as mobile phase additives. Green Chem 2011; 13: 115 – 126.
- S. Kawano, T. Kida, K. Miyawaki, Y. Noguchi, E. Kato, T. Nakano, M. Akashi. Cyclodextrin polymers as highly effective adsorbents for removal and recovery of polychlorobiphenyl (PCB) contaminants in insulating oil. Environ Sci Technol 2014; 48: 8094 – 8100.
- Alsbaiee A, Smith BJ, Xiao L, Ling Y, Helbling DE, Dichtel WR. Rapid removal of organic micropollutants from water by a porous β-cyclodextrin polymer. Nature 2016; 529: 190 – 194.
- Bhattarai B, Muruganandham M, Suri RPS. Development of high efficiency silica coated β-cyclodextrin polymeric adsorbent for the removal of emerging contaminants of concern from water. J Hazard Mater 2014; 273: 146 – 154.
- Zhoua Y, Cheng G, Chen K, Lu J, Lei J, Pu S. Adsorptive removal of bisphenol A, chloroxylenol, and carbamazepine from water using a novel β-cyclodextrin polymer. Ecotox Environ Safe 2019; 170: 278 – 285.
- Tang P, Sun Q, Zhao L, Tang Y, Liu Y, Pu H, Gan N, Liu Y, Li H. A simple and green method to construct cyclodextrin polymer for the effective and simultaneous estrogen pollutant and metal removal. Chem Eng J 2019; 366: 598 – 607.
- Bragança de Carvalho L, Garcia Carvalho T, Magriotis ZM, Castro Ramalho T, Matos Alves Pinto L. Cyclodextrin/silica hybrid adsorbent for removal of methylene blue in aqueous media. J Incl Phenom Macrocycl Chem 2014; 78: 77 – 87.
- Wang S, LI Y, Fan X, Zhang F, Zhang G. β-Cyclodextrin functionalized graphene oxide: an efficient and recyclable adsorbent for the removal of dye pollutants. Front Chem Sci Eng 2015; 9: 77 – 83.
- Shao D, Sheng G, Chen C, Wang X, Nagatsu M. Removal of polychlorinated biphenyls from aqueous solutions using β-cyclodextrin grafted multiwalled carbon nanotubes. Chemosphere 2010; 79: 679 – 685.
- Zhang F, Wu W, Sharma S, Tong G, Deng Y. Synthesis of cyclodextrin-functionalized cellulose nanofibril aerogel as a highly effective adsorbent for phenol pollutant removal. BioResources 2015; 10: 7555 – 7568.
- Qin X, Bai L, Tan Y, Li L, Song F, Wang Y. β-Cyclodextrin-crosslinked polymeric adsorbent for simultaneous removal and stepwise recovery of organic dyes and heavy metal ions: Fabrication, performance and mechanisms. Chem Eng J 2019; 372: 1007 – 1018.
- Zhao F, Repo E, Yin D, Meng Y, Jafari S, Sillanpäa M. EDTA-Cross-Linked β‑Cyclodextrin: An Environmentally Friendly Bifunctional Adsorbent for Simultaneous Adsorption of Metals and Cationic Dyes. Environ Sci Technol 2015; 49: 10570 – 10580.