Page 30 - Demo
P. 30
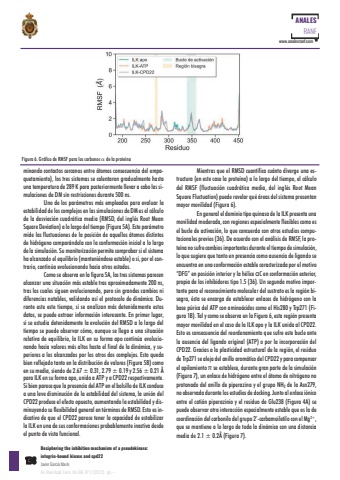
mientrasqueelrmsDcuantificacuántodivergeunaestructura(enestecasolaproteína)alolargodeltiempoelcálculodelrmsF(fluctuacióncuadráticamediadelinglésrootmeansquareFluctuation)puederevelarquéáreasdel sistemapresentanmayormovilidad(Figura6)engeneraleldominio tipoquinasadelaILKpresentaunamovilidadmoderadaconregionesespecialmente flexiblescomoeselbucledeactivaciónloqueconcuerdaconotrosestudioscomputacionalesprevios(36)DeacuerdoconelanálisisdermsF,laproteínano sufrecambiosimportantesduranteel tiempode simulaciónloquesugierequetantoenpresenciacomoausenciadeligandoseencuentraenunaconformaciónestablecaracterizadaporelmotivoDFGenposicióninteriorylahéliceαcenconformaciónexterior,propiadelosinhibidorestipo15(36)UnsegundomotivoimportanteparaelreconocimientomoleculardelsustratoeslaregiónbisagraéstaseencargadeestablecerenlacesdehidrógenoconlabasepúricadelAtPconaminoácidoscomoelHis280ytrp271(Figura1b) tal ycomo seobservaenlaFigura6estaregiónpresentamayormovilidadenelcasodelaILKapoylaILKunidaalcPD22estoesconsecuenciadelreordenamientoquesufreestebucleantelaausenciadelligandooriginal(AtP)oporlaincorporacióndelcPD22Graciasalaplasticidadestructuraldelaregiónelresiduode trp271 sealejadelanilloaromáticodelcPD22 yparacompensarelapilamiento πseestablecedurantegranpartedelasimulación(Figura7)unenlacedehidrógenoentreelátomodenitrógenonoprotonadodelanillodepiperazinayelgruponH2delaAsn279noobservadadurantelosestudiosdedocking JuntoalenlaceiónicoentreelcatiónpiperazinioyelresiduodeGlu238(Figura4A)sepuedeobservarotrainteracciónespecialmenteestablequeesladecoordinacióndelcarbonilodelgrupo 2-carbamoiletiloconelmg2+quesemantienealolargodetodaladinámicaconunadistanciamediade21±02Å(Figura7)minandocontactoscercanosentreátomosconsecuenciadelempaquetamiento)lostressistemassecalentarongradualmentehastauna temperaturade 289Kparaposteriormentellevaracabolas simulacionesdeDmsinrestriccionesdurante500nsUnodelosparámetrosmásempleadosparaevaluarlaestabilidaddeloscomplejosenlas simulacionesdeDmeselcálculodeladesviacióncuadráticamedia(rmsDdelinglésrootmeansquareDeviation)alolargodel tiempo(Figura 5A)esteparámetromidelasfluctuacionesdelaposicióndeaquellosátomosdistintosdehidrógenocomparándolaconlaconformacióninicialalolargodela simulación sumonitorizaciónpermitecomprobar siel sistemahaalcanzadoelequilibrio(manteniéndoseestable)o siporelcontrariocontinúaevolucionandohaciaotrosestadoscomo seobservaenla figura 5Alos tres sistemasparecenalcanzarunasituaciónmásestabletrasaproximadamente200nstrasloscualessiguenevolucionandoperosingrandescambiosnidiferenciasnotablesvalidandoasíelprotocolodedinámicaDuranteesteestetiemposiseanalizanmásdetenidamenteestosdatossepuedeextraerinformacióninteresanteenprimerlugar,siseestudiadetenidamentelaevolucióndelrmsDalolargodeltiemposepuedeobservarcómoaunquesellegaaunasituaciónrelativadeequilibriolaILKensuformaapocontinúaevolucionandohaciavaloresmásaltoshastaelfinaldeladinámicaysuperioresalosalcanzadosporlosotrosdoscomplejosestoquedabienreflejadotantoenladistribuciónde valores(Figura 5b)comoensumediasiendode 267±031 279±019 y 256±021 ÅparaILKen su formaapounidaa AtP yacPD22respectivamentesibienparecequelapresenciadel AtPenelbolsillodeILKconduceaunalevedisminucióndelaestabilidaddelsistemalaunióndelcPD22produceelefectoopuestoaumentandolaestabilidad ydisminuyendo su flexibilidadgeneralen términosdermsDestoesindicativodequeelcPD22parecetenerlacapacidaddeestabilizarlaILKenunadesusconformacionesprobablementeinactivadesdeelpuntodevistafuncional138ANALESRANFwwwanalesranfcomDecipheringtheinhibitionmechanismofapseudokinaseintegrin-boundkinaseandcpd22JavierGarcíaMarínAnRealAcadFarmVol88Nº2(2022)·pp---Figura6GráficodermsFparaloscarbonosadelaproteína