Page 45 - 86_01
P. 45
ANALES
RANF
www.analesranf.com
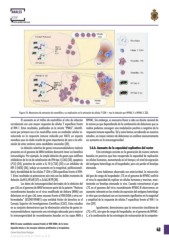
Figura 10: Mecanismo de activación de neutrófilos y su implicación en la activación de células T CD8+ tras la infección por NYVAC-C o NYVAC-C ?3.
El aumento en el tráfico de neutrófilos al sitio de infección NYVAC. Sin embargo, es necesario llevar a cabo un diseño racional de
correlacionó con una mayor respuesta de células T específicas frente la misma ya que dependiendo de la combinación de deleciones que se
al VIH-1. Estos resultados, publicados en la revista “PNAS”, identifi- realice podemos conseguir una modulación positiva o negativa de la
caron por primera vez a los neutrófilos como un mediador celular in- respuesta inmune específica. Tal y como hemos corroborado en nuestros
volucrado en la respuesta inmune inducida por VACV, un aspecto estudios, un mayor número de deleciones no conlleva necesariamente
novedoso que sin duda resulta de gran importancia de cara a la utili- un aumento en la inmunogenicidad.
zación de estos vectores como candidatos vacunales (32).
2.6.b. Aumento de la capacidad replicativa del vector
La deleción selectiva de genes inmunomoduladores todavía Esta estrategia consiste en la generación de nuevos vectores
presentes en el genoma de MVA también demostró tener un beneficio
inmunológico. Por ejemplo, la simple deleción de genes que codifican basados en poxvirus que han recuperado la capacidad de replicación
inhibidores de la vía de señalización de IFN tipo I (C6L) (33), apoptosis en células humanas, aumentando así el tiempo y el nivel de expresión
(F1L) (34), proteína de unión a IL-18 (C12L) (35) o un inhibidor de del antígeno heterólogo en el hospedador, pero sin perder el fenotipo
IRF-3 (N2L) (36), indujo un aumento en la magnitud, polifuncionali- atenuado.
dad y durabilidad de las células T CD4 y CD8 específicas frente al VIH-
1. Estos resultados se potenciaron aún más con los dobles mutantes de Como habíamos observado con anterioridad, la reinserción
deleción ?A41L/B16R (37) o ?C6L/K7R (38). del gen de rango de hospedador C7L en el genoma de NYVAC confirió
al virus la capacidad de replicar en células humanas y murinas, man-
Los datos de inmunogenicidad derivados de la deleción del teniendo un fenotipo atenuado in vivo. Cuando reinsertamos el gen
gen C6L en el genoma de MVA formaron parte de la patente “Vectores C7L en el genoma del virus recombinante NYVAC-B observamos un
recombinantes basados en el virus modificado de Ankara (MVA) con aumento relevante en los niveles de expresión del antígeno heterólogo
deleciones en el gen C6L como vacunas frente al VIH/SIDA y otras en- in vitro que correlacionó con un incremento significativo en la magnitud
fermedades” (ES2401904B1) cuya entidad titular de derechos es el y amplitud de la respuesta de células T específicas frente al VIH-1 in
Consejo Superior de Investigaciones Científicas (CSIC). Estos estudios vivo (39).
en su conjunto demostraron que la eliminación selectiva de genes in-
munomoduladores representa una estrategia adecuada para mejorar Igualmente, demostramos que la reinserción simultánea de
la inmunogenicidad de recombinantes basados en las cepas MVA y C7L y K1L, otro gen de rango de hospedador, en el genoma de NYVAC-
C, o la combinación de las estrategias de restauración de la competen-
MVA-B como candidato vacunal frente al VIH/SIDA: de la inves- 43
tigación básica a los ensayos clínicos profiláctico y terapéutico.
Carmen Elena Gómez Rodríguez
An Real Acad Farm Vol. 86. Nº 1 (2020) · pp. 29 -60