1. INTRODUCCIÓN: FABRICACIÓN POR LOTES Y FABRICACIÓN EN CONTINUO
La Industria Farmacéutica ha constituido un ejemplo de implantación y mejora de procesos de fabricación, manteniendo como eje central la CALIDAD DEL PRODUCTO FINAL, lo que se ha traducido en una filosofía de mejora continua. Tradicionalmente, este objetivo de calidad del medicamento se ha perseguido a través de la estrategia de fabricación por lotes (1). Este modo de trabajar parece el más lógico si consideramos que fabricamos una cantidad fija y siempre igual de un medicamento, mediante procedimientos previamente definidos de operaciones de fabricación y de control, tanto en proceso como en producto terminado. Dicho control sobre producto terminado condiciona la liberación de un lote al mercado en función del cumplimiento de una serie de criterios y requisitos de calidad previamente establecidos. Además, el hecho de trabajar con un concepto de lote facilita la traza de un medicamento y su posible retirada en caso necesario.
Las Guías de Normas de Correcta Fabricación de Medicamentos de Uso Humano y Veterinario (EU Guidelines for Good Manufacturing Practice for Medicinal Products for Human and Veterinary Use), disponibles en la base de datos de acceso público EUDRALEX (2), establecen que el seguimiento de la calidad del medicamento comprende el ciclo de vida completo del medicamento, desde la fase de ensayos clínicos hasta la retirada final del producto (3). La normativa europea aconseja la incorporación al mencionado proceso de seguimiento de la calidad de las indicaciones de otras guías internacionales, como las de la Conferencia Internacional de Armonización de Requisitos Técnicos para el Registro de Medicamentos de Uso Humano, conocidas comúnmente como guías ICH. En concreto, las guías ICH Q9 e ICH Q10, centradas en la calidad farmacéutica y en la gestión de riesgos (4, 5), recomiendan la integración de las normas de calidad farmacéutica con los conceptos de calidad globales definidos en la norma ISO 9001:2015, generalmente aceptada como el “estándar de oro” de las normas de gestión de calidad (3, 6).
En las guías GMP europeas, se define el concepto de LOTE como “una cantidad definida de materia prima, material de acondicionamiento o producto procesado en uno o múltiples etapas del que se espera que sea homogéneo”, si bien incluye una aclaración indicando que “en el caso de fabricación en continuo, el concepto de lote debe corresponder a una fracción definida de la producción, caracterizada por un grado de homogeneidad definido” (6). En el anexo 1 de la Directiva 2001/83/EC, revisada por la Directiva 2003/63/EC (8), se especifica expresamente la siguiente definición orientada a efectos de control del producto terminado: “Un lote de un medicamento comprende todas las unidades de una forma farmacéutica que provengan de una misma cantidad inicial de material y hayan sido sometidas a la misma serie de operaciones de fabricación y esterilización o, en el caso de un proceso de producción continuo, el conjunto de unidades fabricadas en un lapso de tiempo determinado”. Como podemos observar, en las definiciones actualizadas ya se introduce una posibilidad de establecer un tipo de lote basado en la fabricación en continuo.
En 2016, el Subcomité de Fabricación Avanzada de la secretaría de estado de la que depende la política científica en Estados Unidos marcaba las áreas prioritarias financiables de investigación y desarrollo para los siguientes años. En el sector farmacéutico, se plantearon varias líneas estratégicas de I+D, como la necesidad de profundizar en la fabricación de medicamentos de origen proteico, fabricación de principios activos a demanda o la incorporación de la filosofía de fabricación en continuo. En 2019, con la crisis sanitaria desencadenada por la pandemia COVID-19, se evidenció la necesidad de desarrollar estrategias de fabricación de medicamentos a gran escala y con procesos de desarrollo rápidos y eficaces (9).
Los retos planteados en la última década, encaminados a una mejora en la automatización de procesos y en conseguir métodos de fabricación más rápidos, sostenibles y eficaces, han supuesto un aumento del interés de la Industria Farmacéutica por la implantación de la estrategia basada en la fabricación en continuo. Si bien se ha venido centrando su gestión de riesgos y de calidad en procedimientos basados en la CALIDAD POR ENSAYO, conocida por sus iniciales QbC (Quality by Control), han aparecido nuevos enfoques basados en estrategias de CALIDAD POR DISEÑO (QbD – Quality by Design) y en la TECNOLOGÍA ANALÍTICA DE PROCESOS (PAT- Process Analytical Technology) (9). Estas nuevas herramientas han hecho posible que la fabricación continua de medicamentos sea ya una realidad y existen numerosos ejemplos de procesos en continuo ya aprobados. Uno de los ejemplos más significativos de esta nueva tendencia, que supuso un hito en la implantación de la fabricación en continuo, es la aprobación en 2015 por parte de la FDA y de la EMA de Orkambi®, el primer comprimido obtenido mediante esta tecnología, lo que abrió la senda para posteriores autorizaciones como Prezista® en 2016, Verzenio® en 2017 o Daurismo® en 2018, entre otros (1, 10-14). Para ello se han tenido que superar una serie de falsos mitos como los siguientes:
- “La fabricación en continuo solo es útil para volúmenes de producción que exceden la capacidad de los procesos farmacéuticos”, lo que se contradice con las actuales evidencias de la utilidad de esta tecnología en todo tipo de tamaños de fabricación en cuanto a ahorro de tiempo y coste de procesos de control.
- “La fabricación en continuo no es una estrategia apropiada cuando el tipo de producto fabricado cambia con una alta frecuencia”, afirmación que hoy día carece de fundamento, ya que se ha demostrado que, en aquellos procesos de fabricación en continuo implantados, la agilidad para incorporar cambios es mucho mayor que en los tradicionales procesos por lotes.
- “Un proceso de fabricación en continuo no puede reproducir los niveles de calidad requeridos por la industria farmacéutica”, aseveración totalmente rebatida por los numerosos ejemplos de medicamentos ya aprobados que se elaboran mediante esta tecnología.
- “La dificultad de validación y el escepticismo por parte de las agencias reguladoras pueden retrasar la puesta en comercialización del producto”. A este respecto, se ha visto que un proceso que es controlado mediante una tecnología analítica de procesos (PAT) es mucho más ágil y eficaz a la hora de realizar validaciones de cualquier modificación en las operaciones de producción. Como se ha comentado anteriormente, el gran número de medicamentos aprobados por las agencias reguladoras como FDA y EMA que hoy día han adoptado la fabricación en continuo desmonta este argumento.
No fue hasta 2019 cuando el Departamento de Salud de la FDA publicó el borrador de una guía (Docket No. FDA–2019–D–0298) para la implantación de procesos de fabricación en continuo (15), basándose en las evidencias del conocimiento acumuladas hasta ese momento y en la publicación previa de una guía de la Sociedad Americana para Ensayos y Materiales (American Society for Testing and Materials – ASTM) en 2016 sobre aplicación de verificación de procesos en continuo para fabricación farmacéutica y biofarmacéutica, guía que se ha revisado por última vez en octubre de 2024 y constituye uno de los documentos de referencia en el marco regulatorio que afecta a esta tecnología (16).
El Consejo Internacional de Armonización de los Requisitos Técnicos de los Medicamentos de Uso Humano (ICH) publicó en 2021 el borrador de una guía dirigida a sentar base regulatoria internacional en lo tocante a la fabricación en continuo. El texto definitivo para esta guía aprobada vio la luz finalmente en noviembre de 2022 con el título original “ICH Q13 – Continuous Manufacturing of Drug Substances and Drug Products”.
(17). En este documento se definen y describen conceptos regulatorios clave como el “estado de control”, “validación de proceso”, “verificación en continuo”, “lote”, “frecuencia de monitorización”, “trazabilidad”, así como otros aspectos relacionados con la gestión de no conformidades, validaciones de procesos de limpieza, lote de registro, liberación paramétrica o tecnología analítica de procesos (PAT), etc.
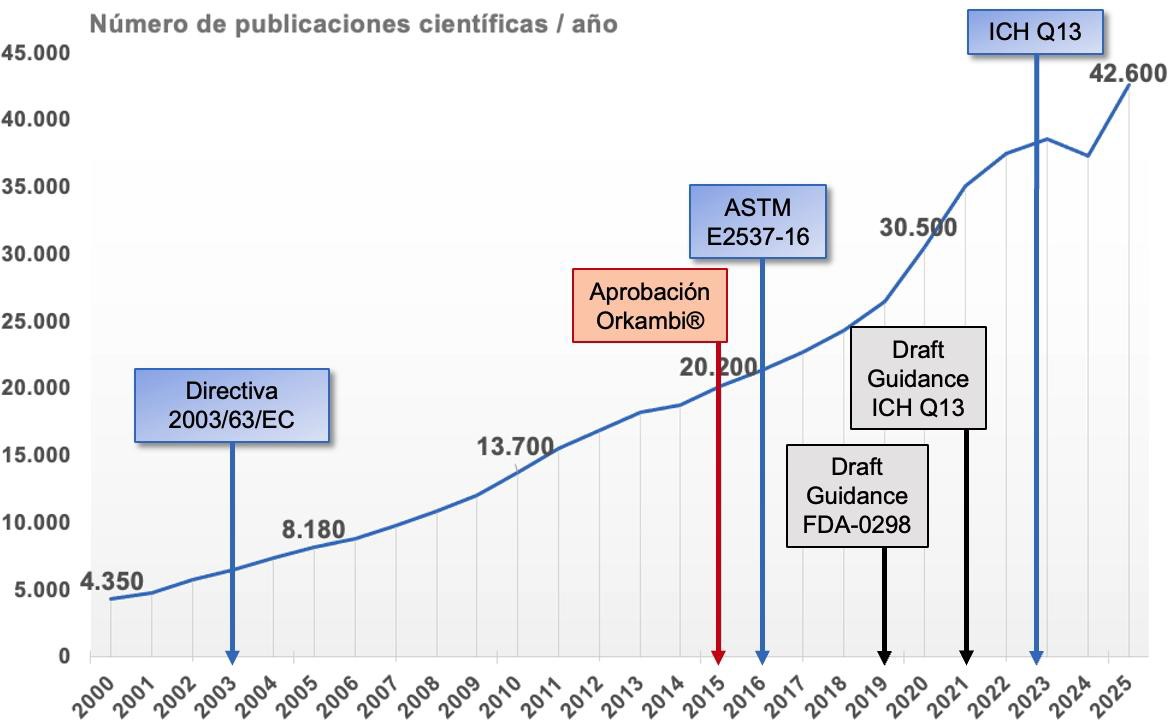
Haciendo una revisión del volumen de literatura científica aparecida en las últimas décadas sobre “Pharmaceutical continuous manufacturing”, se observa la tendencia representada en la figura 1, en la que también se marcan los hitos principales en el desarrollo e implantación de la fabricación en continuo.
Figura 1. Evolución del número de publicaciones científicas (datos extraídos de Google Académico) sobre “pharmaceutical continuous manufacturing” desde el año 2000 hasta la actualidad.
Como podemos observar, en el último año se ha multiplicado casi por diez el número de publicaciones científicas con respecto al número registrado en el año 2000. Además, se observa que el interés científico de la fabricación en continuo registra una tendencia creciente con una pendiente constante media que se interpreta como un incremento sostenido medio de aproximadamente 1.500 publicaciones/año. Esta tendencia se sostiene sobre las novedades técnicas y regulatorias surgidas, sobre todo a partir de la directiva 2003/63/EC, que ya introducía el embrión de lo que posteriormente se plasmaría en un marco legislativo consolidado.
Si analizamos los datos numéricos en profundidad, se observan dos fases diferenciadas. En la primera etapa comprendida entre los años 2000 y 2015, se observa un incremento interanual de aproximadamente 1.100 publicaciones. A partir de 2015, cuando se publica la noticia de la aprobación de los primeros medicamentos fabricados en continuo, la tendencia se dispara, alcanzándose un incremento medio interanual de unas 2500 publicaciones nuevas por año.
Otra conclusión que se deriva de la observación de estos datos es que el interés científico sobre esta tecnología en modo alguno ha tocado techo: si bien en 2024 se registra una ligera caída, probablemente derivada de la publicación ya definitiva de ICH Q13, que acaba definiendo y acotando un gran número de conceptos, se registra una recuperación de nuevo en 2025, considerando incluso que en este último año aún no está concluido a la fecha de recopilación de datos que incluye hasta el mes de octubre.
Los principales conceptos definidos en la normativa consolidada a través de la guía ICHQ13 son los siguientes:
- Controles de Proceso Activo (Active Process Controls): sistema de diseño de hardware y software, mecanismos y algoritmos que ajustan el funcionamiento de un proceso de forma automática para mantener el producto final dentro de unas especificaciones definidas.
- Perturbaciones: modificaciones no planificadas en parámetros de entrada del proceso que exceden los límites de especificaciones normales operativas, como parámetros de proceso inesperados, propiedades de materias primas que salen del intervalo de especificaciones de aceptación, parámetros de equipos inesperados, etc., que se introducen en el sistema.
- Desviación de materiales: procedimientos para aislar o separar materiales del flujo de producción en el proceso en continuo.
- Trazabilidad de materiales: capacidad para rastrear un material a lo largo del proceso de fabricación.
- Mantenimiento del modelo: Conjunto de actividades planificadas durante el ciclo de vida del producto con el fin de analizar y mantener el rendimiento del modelo y garantizar su idoneidad de manera continua para el propósito previsto y aprobado.
- Dinámica del proceso: respuesta de un proceso de fabricación a cambios en las entradas o condiciones, o a posibles eventos transitorios.
- Distribución del tiempo de residencia (RDT): medida del intervalo de tiempos de residencia que experimenta un material al pasar por un entorno de proceso, recipiente u operación unitaria específica.
- Tiempo de ejecución (RT): tiempo necesario para obtener una cierta cantidad de producto de salida.
- Sensor virtual: modelo que se utiliza en lugar de la medición física para estimar una variable o atributo (p. ej., un atributo de calidad de un material) a partir de datos obtenidos por mediciones reales (p. ej., datos de proceso). El desarrollo del modelo, incluida la selección de dichas variables de datos, se basa en un conocimiento integral tanto del proceso como del producto y del proceso.
- Estado estacionario: estado definido por una condición estable que se mantiene inalterada y sin cambios a lo largo del tiempo.
- Evento transitorio: condición temporal en la que un proceso experimenta un cambio dinámico, que puede ser debido a una perturbación o a una alteración intencionada de las condiciones operativas seleccionadas (p. ej., arranque, parada, cambios de una condición operativa a otra).
- Operación unitaria: etapa básica de un proceso que conlleva una transformación física, química o biológica (p. ej., una reacción química, un proceso de cristalización, una etapa de filtración, mezcla, granulación, compresión, pero también un proceso de cultivo celular, una purificación o una inactivación de virus).
Entre los conceptos que quedan definidos en la normativa, destaca por su importancia el de LOTE. Según la guía ICH Q13, la definición previamente dada en la ICH Q7 es perfectamente aplicable a la fabricación en continuo, tanto de principios activos como de medicamentos. Según esto, el tamaño de lote en un procedimiento en continuo se define a partir de las cantidades de materiales de partida, de la cantidad de producto final o del tiempo definido por un flujo operacional definido.
A pesar de lo expuesto, se admiten algunas alternativas, como por ejemplo definir el tamaño de lote en términos de intervalo. Por ejemplo, definiendo el tiempo mínimo y máximo de producción o el número mínimo y máximo de unidades producidas. En este caso, debe justificarse el método por el que se establece dicho intervalo, de forma que una modificación de tamaño de lote dentro del intervalo aprobado es una cuestión gestionada internamente desde el propio Sistema de Calidad Farmacéutica (PQS por sus iniciales en inglés). Sin embargo, cualquier cambio de tamaño de lote que sobrepase los límites del intervalo definido en su aprobación inicial debe justificarse de manera clara y consistente y sufrir un proceso de aprobación previa por parte de la autoridad regulatoria.
Según lo explicado anteriormente, es necesario establecer un procedimiento de medida con unos criterios de aceptación claramente definidos en el Sistema de Calidad Farmacéutica que permitan establecer los parámetros comparativos de consistencia entre lotes y de robustez del sistema. En todo caso, el procedimiento que se escoja para definir el tamaño de lote debe quedar perfectamente descrito en el dosier de autorización.
En definitiva, no sería del todo correcto abordar la implantación de un proceso de fabricación en continuo como un cambio desde una fabricación por lotes, sino que supondría una redefinición del concepto de lote.
En el apartado 4.6 de la guía se especifica la filosofía a seguir para pasar de un proceso de fabricación “por lotes” a una “fabricación en continuo”. En general, se destaca la necesidad de desarrollar una estrategia de control adecuada, de modo que el producto final obtenido mediante fabricación en continuo presente una calidad comparable a la del elaborado mediante fabricación por lotes. Debe usarse un enfoque científico y técnico basado en análisis de riesgos para establecer de manera adecuada la comparación antes mencionada y valorar la necesidad de realizar estudios adicionales de bioequivalencia, estudios no clínicos o clínicos, así como datos de estabilidad. La guía ICH Q13 recomienda encarecidamente solicitar la aprobación regulatoria antes de implementar la conversión de un proceso por lotes aprobado a un proceso continuo, pudiendo consultar con la autoridad regulatoria para aclarar las expectativas regulatorias y la aceptabilidad de su estrategia y la documentación presentada para los cambios propuestos (por ejemplo, cuándo son necesarios cambios potenciales en la formulación para permitir la conversión a un proceso continuo y el impacto de estos cambios en el registro del producto).
2. MODERNAS HERRAMIENTAS PARA LA IMPLANTACIÓN Y MEJORA DE SISTEMAS DE PRODUCCIÓN EN CONTINUO.
Si analizamos la evolución de la tecnología en los procesos industriales, podemos hablar de cuatro fases claramente definidas (18, 19):
- Industria 1.0: primer paso de la evolución de la industria farmacéutica, definida a lo largo del S. XIX por el cambio de escala de producción manual de medicamentos al desarrollo de maquinaria industrial, capaz de aumentar los niveles de producción y de homogeneizar las características del producto final. Este salto fue posible a partir de farmacias de las que nacieron incipientes instalaciones de fabricación a escala industrial de medicamentos.
- Industria 2.0: etapa definida por la irrupción de la electricidad que trajo consigo el desarrollo de maquinaria más eficiente y con un grado de automatización superior. En esta etapa se implantan los primeros sistemas de control pasivo, basados en la observación de ciertos parámetros de fabricación.
- Industria 3.0: Esta tercera revolución industrial viene marcada por la revolución tecnológica basada en los avances en informática, comunicación e internet que ha posibilitado un mayor grado de automatización de procesos y equipos. Esto ha servido para profundizar en las tecnologías de automatización de los procesos productivos y de control y poder definir así conceptos como el de la fabricación en continuo.
- Industria 4.0: Basada en los avances de la etapa anterior, esta cuarta revolución industrial supone una mejora y perfeccionamiento en la creación de algoritmos y otras herramientas como el control y garantía de calidad de procesos en continuo (19-24) que permiten un manejo de gran cantidad de datos en tiempo real en la creación de sistemas productivos que se autocontrolan y se autorregulan, basados en la aún hoy incipiente irrupción de la inteligencia artificial.
El cambio de paradigma en el concepto de lote anteriormente descrito plantea una serie de retos importantes en el sentido de que se necesita implantar un sistema de control continuo en tiempo real desde el Sistema de Calidad Farmacéutica para asegurar la homogeneidad entre lotes y el mantenimiento de un nivel de calidad adecuado en el producto final. Es lo que se conoce como “monitorización continua de parámetros críticos de proceso” (CPP por sus iniciales en inglés). Es, por tanto, necesario tener la capacidad de medir en tiempo real, a lo largo del flujo de producción, atributos y parámetros que definen la calidad de materias primas de partida, productos intermedios y producto final usando lo que se conoce como TECNOLOGÍA ANALÍTICA DE PROCESOS (PAT por sus iniciales en inglés) (25).
La PAT se basa en la incorporación de técnicas analíticas que permiten proporcionar datos sobre la calidad del producto a lo largo de la cadena de producción de una manera rápida y no destructiva. Técnicas como la espectroscopía de infrarrojo cercano (NIR) o la espectroscopía RAMAN han ganado una gran notoriedad por su rapidez de respuesta y su sensibilidad. Ambas técnicas son complementarias desde la perspectiva de que presentan una sensibilidad distinta para según qué grupos funcionales, siendo la espectroscopía NIR más sensible para enlaces polares y estados vibracionales asimétricos y la RAMAN más útil para la detección y cuantificación de moléculas con grupos apolares y con estados vibracionales simétricos (25-28).
Otras técnicas que han ganado gran notoriedad por su posibilidad de servir como sondas –PAT– son, por ejemplo, la IMAGEN POR PULSOS TERAHÉRTZICOS (TPI), que se ha mostrado especialmente útil para medir el grosor de una cubierta polimérica y su evolución a lo largo de un proceso de recubrimiento pelicular de comprimidos, mediante cambios en la refractividad de un haz de luz láser que incide sobre la muestra (29, 30). Otro ejemplo de técnica capaz de medir en tiempo real el grosor de una película aplicada es la TOMOGRAFÍA DE COHERENCIA ÓPTICA (OCT), basada en el fenómeno de interferencia de baja coherencia de las ondas de luz que se reflejan tras penetrar en la muestra (31).
El ANÁLISIS DE IMAGEN MULTIESPECTRAL UV constituye otro ejemplo de técnica aplicable como sonda PAT, ya que proporciona información en tiempo real sobre la distribución de distintos compuestos en el lecho de una muestra mediante el uso de diferentes filtros que permiten analizar la imagen ultravioleta a diferentes longitudes de onda (32-34), lo que permite obtener parámetros indicativos de homogeneidad de una mezcla, distribución de un polímero en un proceso de recubrimiento, etc.
Las técnicas anteriormente mencionadas son ejemplos de sondas – PAT que nos permiten obtener datos en tiempo real a lo largo de un proceso continuo de fabricación de medicamentos en diferentes formas farmacéuticas, pero si consideramos la incorporación de la estrategia de fabricación en continuo en la síntesis y purificación de principios activos, las posibilidades son aún mayores. En estos casos se están empezando a implantar técnicas basadas en la espectroscopía RAMAN, resonancia magnética nuclear o espectrometría de masas, entre otras. Esto ha permitido incorporar a la ecuación, no solo la estrategia PAT, sino la posibilidad de desarrollar ALGORITMOS DE AUTOOPTIMIZACIÓN DE PROCESOS (35-37), lo que supone un notable avance en la creación de sistemas productivos automatizados y autoajustables en función de las posibles desviaciones halladas y en la predicción de las mismas.
No es posible analizar el grado de implantación actual ni la evolución de la estrategia de fabricación en continuo sin analizar la influencia de la irrupción de la INTELIGENCIA ARTIFICIAL. Son numerosos los estudios que plantean la aplicación de la IA en este aspecto. Ya en 2020 y 2021 aparecen diversos intentos de predecir el impacto de la IA (38-40). Recientes estudios de revisión (41) evidencian que la IA es ya, hoy en día, una herramienta capaz de detectar desviaciones y proponer correcciones y modificaciones en procesos de fabricación, empaquetado y control de calidad, manteniendo niveles de control de calidad fiables a lo largo del proceso de producción en continuo, siendo capaz de predecir posibles riesgos, anticipándose a los procesos de mantenimiento de equipos, etc. Se constituye, por tanto, la AI en una prometedora herramienta que proporciona a las empresas industriales del sector farmacéutico una mejora en la capacidad de tomar decisiones estratégicas. Es difícil predecir a día de hoy hasta qué punto la IA transformará los procesos de fabricación industrial de medicamentos, y la fabricación en continuo se aprovecha ya de esta herramienta para mejorar la capacidad y agilidad productiva.
3. GRANULACIÓN HÚMEDA EN CONTINUO MEDIANTE TORNILLOS GEMELOS CO-ROTATORIOS
Uno de los recursos galénicos habituales en la elaboración de comprimidos o cápsulas rígidas es la granulación. Mediante este proceso, se pretende transformar una mezcla pulverulenta con malas propiedades de flujo, problemas de segregación, deficiente capacidad de compactación, con tendencia al apelmazamiento o simplemente con riesgo elevado de generar aerosoles en fábrica, en agregados sólidos de partículas individuales con unas adecuadas propiedades mecánicas para su manipulación posterior. De manera general, los problemas de las mezclas anteriormente comentados pueden ser achacados a diferencias significativas en las distintas propiedades físicas de las partículas implicadas, tales como tamaño, cristalinidad, porosidad, carga eléctrica, densidad real y aparente, geometría, rugosidad o humedad en equilibrio, entre otras.
Existen diversas técnicas de fabricación de granulados, entre las que destacan en la industria farmacéutica la granulación húmeda y la granulación seca. La granulación húmeda implica la adición sobre la mezcla pulverulenta de disolventes puros o mezclas de estos, para facilitar la incorporación y distribución de los aglutinantes en el lecho pulverulento o disolver componentes de la mezcla que, tras la eliminación de los líquidos, faciliten la generación de puentes sólidos estables entre las partículas. Por su parte, la granulación seca supone la compactación a alta presión de la mezcla para su posterior fragmentación. En este caso es habitual incorporar mayor proporción de aglutinantes o excipientes más potentes. Aunque cada modalidad tiene sus ventajas e inconvenientes, ambos sistemas necesitan de posteriores procesos de molienda, selección del rango de tamaño adecuado y lubricación de las partículas obtenidas. En general, la granulación húmeda es la técnica más habitual a nivel industrial por su versatilidad y experiencia de uso, lo que facilita la identificación de variables críticas en el proceso y permite lograr el espacio de diseño de la formulación de manera sencilla.
Desde un punto de vista práctico, los principales mecanismos de enlace entre partículas sólidas son los siguientes (42):
- Fuerzas de cohesión en películas de líquidos inmóviles como consecuencia de la disponibilidad de moléculas de agua en la superficie de las partículas en cantidad suficiente como para formar una película continua. Esta película es capaz de disminuir la distancia entre las partículas e incrementar el área de contacto interparticular, favoreciendo la cohesión mediante fuerzas de van der Waals. Es responsable de la adhesión de mezclas en presencia de humedad. En el caso de que el agua contenga moléculas de aglutinante disueltas, las fuerzas de cohesión pueden ser elevadas.
- Fuerzas interfaciales en películas de líquidos móviles. Cuando la cantidad de líquido se incrementa lo suficiente para dejar de ser una película inmóvil superficial, se crean puentes líquidos entre las partículas debido a la presión capilar y a fuerzas interfaciales. Aunque reversibles tras el secado, estas uniones preceden a la formación de puentes sólidos formados por los aglutinantes y otras sustancias disueltas en el líquido de granulación.
Por eso es fundamental la disposición del aglutinante en la superficie de la partícula, para formar uniones con otras partículas. El proceso de aglomeración puede ser considerado como un paso entre un sistema trifásico (aire-líquido-sólido), en el que la mayoría de las partículas se encuentran en el estado pendular, y un sistema bifásico (líquido-sólido), en el que las partículas se ensamblan en un estado capilar. Si seguimos incorporando agua, las fuerzas capilares desaparecen y solo la tensión superficial mantiene unida la gota, desapareciendo por tanto las fuerzas interfaciales. Flemmer consideró para esferas lisas que el contenido en humedad entre estos estados sería: régimen pendular (0–13,5%), funicular (13,6-99%) y capilar (100%). La fuerza de unión de un aglomerado según la ecuación de Rumpf dependería de la porosidad y del diámetro de las partículas, de la fuerza de unión de un único puente entre dos partículas y del número de puentes de contacto entre ambas (43). La fuerza de unión de un puente entre dos partículas depende de la suma de la fuerza capilar de succión y de la tensión superficial del líquido. El máximo grado de unión del aglomerado se consigue al estado capilar. A partir de ahí, si seguimos incorporando agua, obtendríamos una gota con partículas en suspensión que se mantendría exclusivamente por la tensión superficial del solvente. Un aspecto a considerar en la calidad del gránulo final como consecuencia de estas fuerzas de cohesión es la migración intragranular de componentes más solubles como consecuencia de la mayor presión de succión y del incremento del área de contacto entre gránulos. Cuanto mayor es la superficie específica, mayor es este efecto. Durante el amasado, para una cantidad fija de líquido, la fuerza de cohesión, la densidad y el contenido en humedad se incrementan con el tiempo, hasta un punto en que la fuerza de cohesión cae como consecuencia de un “efecto lubrificante” del líquido. En ese momento, la masa se comportaría como una pasta.
Formación de puentes sólidos: Se pueden formar por reacciones químicas entre componentes de la mezcla, cristalización de sustancias disueltas, solidificación de componentes fundidos o endurecimiento de aglutinantes. En procesos de alta cizalla y como consecuencia de la fricción entre partículas o por el elevado aporte externo de energía, pueden producirse incrementos locales de temperatura y presión que pueden favorecer estos procesos.
Atracción entre partículas sólidas y entrelazamiento mecánico: Aunque menos importante en comparación con los mecanismos anteriores, la atracción entre partículas sólidas y fenómenos de entrelazamiento entre partículas irregulares puede contribuir en ocasiones de manera significativa a la formación de un gránulo denso y de buenas propiedades mecánicas.
En la granulación húmeda, el mecanismo de agregación de partículas predominante es la formación de puentes líquidos que se establecen entre partículas sólidas y la posterior formación de puentes sólidos; si bien, inicialmente y al final del proceso, también es interesante la contribución de las fuerzas de van der Waals y electrostáticas entre partículas sólidas. El gránulo inicial consiste en partículas humedecidas que forman aglomerados por puentes líquidos. Las fuerzas de amasado en los granuladores hacen que la distancia entre partículas se reduzca y se densifique el aglomerado y, si la cantidad de agua es suficiente, se saturen los poros entre partículas. Las fuerzas de cizalla pueden romper estos puentes líquidos. Por lo general, se considera que la granulación húmeda es un equilibrio entre aglomeración y rotura de partículas. Por tanto, para iniciar la granulación debe formarse un núcleo inicial, seguido de una consolidación y coalescencia entre gránulos. La formación de gránulos puede ser debida también a la coalescencia de varios aglomerados. Este tipo de gránulos presentan un ligero exceso de humedad en superficie y cierta plasticidad. Gránulos más secos no serán capaces de realizar estos mecanismos de coalescencia, aunque sí serán capaces de captar en superficie partículas de menor tamaño.
Tradicionalmente, la industria farmacéutica ha trabajado con lotes, es decir, cantidades previamente definidas de materias primas, que son transformadas en un lote homogéneo de medicamentos. En los últimos años, sin embargo, existe un interés creciente en nuestro sector por la introducción de procesos continuos debido a su capacidad de producción solo limitada por el tiempo de funcionamiento del sistema (esto lo hace especialmente interesante tanto para grandes producciones como para lotes clínicos y subclínicos), ausencia de complejos procesos de escalado por concepto, robustez de los procesos en total sintonía con las actuales recomendaciones de la normativa 21-CFR y las guías QbD de la EMA, reducción de costos productivos (mano de obra, materias primas, equipos y espacio), facilidad de automatización por la aplicación de técnicas analíticas en línea (PAT) y, en general, por el incremento del rendimiento de las líneas de producción. En granulación, la vía seca mediante cilindros compactadores es un buen ejemplo de esta tendencia. En el caso de la granulación húmeda, los procesos son más complejos, pudiendo hablar de sistemas semicontinuos y totalmente continuos.
4. SISTEMAS “CLÁSICOS” DE GRANULACIÓN HÚMEDA EN CONTINUO
4.1. Sistemas de lecho fluido
Los equipos de lecho fluido de granulación húmeda en continuo pueden dividirse en dos categorías, los de celda sencilla y los de celda múltiple. Los primeros surgieron como modificaciones de los equipos tradicionales de lotes adaptados a esta nueva corriente de producción. Para ello, se incorporaron sistemas continuos tanto de alimentación de mezcla como de descarga del granulado. Debido al elevado riesgo de generación de finos por la baja eficacia del proceso, estos equipos suelen equiparse en su descarga con ciclones que permiten devolver, siempre que sea posible por la naturaleza del proceso, las partículas no granuladas al equipo. En estos equipos, debido a que coexisten en un único equipo todas las fases del proceso de formación y consolidación de agregados, el diseño en “sectores” independientes dentro del equipo de los distintos tipos de aire necesarios para el proceso, es crítico. Un ejemplo de esta tecnología son los equipos de la línea AGT de Glatt.
En los equipos de celda múltiple (44), por su parte, la mezcla accede por un lateral del equipo y se desplaza de manera homogénea a través de un plato perforado hacia la zona de descarga, bien por vibración o empujada por corrientes de aire. La geometría de dichas perforaciones hace que se creen microturbulencias de partículas para generar los modelos de flujo adecuados. En cuanto al aire de entrada, este es calefactado o ajustado en su humedad en los distintos compartimentos del equipo en función de la fase de granulación en la que se encuentre cada segmento: precalentamiento y mezclado o humectación, nucleación, crecimiento, secado o enfriamiento de los aglomerados. En cuanto a las boquillas atomizadoras, hay diseños de atomización contracorriente (top-spray como el sistema Glatt CF) o cocorriente (bottom-spray como el sistema Niro), este último para granulados complejos que necesiten aprovechar los fenómenos de sobrehumectación típicos de este diseño. En algunos equipos, el compartimento interior está dividido físicamente en celdas no estancas que facilitan el establecimiento de zonas separadas, mientras que en otros, estas zonas se establecen exclusivamente por el desplazamiento de los aglomerados y por la circulación de aire.
4.2. Sistemas mecánicos
El sistema Glatt MulticellTM es un sistema intermedio entre los sistemas mecánicos y los de lecho fluido. Está formado por un sistema de alimentación y transporte de la unidad granuladora de 4-9 kg, un molino rotatorio, tres lechos fluidos en paralelo (precalentado, calentado y enfriamiento) y un sistema de transporte final para moler y seleccionar los gránulos de los lechos. El tránsito entre los distintos equipos se hace por transporte neumático.
5. SISTEMAS DE GRANULACIÓN HÚMEDA EN CONTINUO POR EXTRUSIÓN
Existen varios diseños de equipos, todos ellos adaptados de la tecnología de extrusión: los extrusores de rodillos, los extrusores de tornillo simple y los extrusores de tornillos gemelos (TSG). Un extrusor industrial, en comparación con los equipos “clásicos” de granulación, es un equipo de tamaño similar a un equipo piloto o incluso galénico. En los extrusores de tornillo, además de los aspectos considerados anteriormente, como la humectabilidad de la mezcla o la aglomeración de partículas, entre otros, es necesario considerar, como consecuencia de su reducido tamaño y precisión de granulación, otros aspectos críticos como la facilidad de eliminar el aire interpuesto entre las partículas, posibles fenómenos de fusión y la refrigeración del sistema. Dado que, salvo en equipos experimentales, los tornillos no están refrigerados, el control de la temperatura ha de hacerse mediante el cuerpo del extrusor. Otro aspecto importante para entender el funcionamiento de estos equipos es considerar que la fricción entre la mezcla y el cuerpo del extrusor es mayor que la fricción entre la mezcla y los tornillos.
Estos equipos vienen acompañados de una o varias tolvas de alimentación dotadas de alimentadores de tornillo sin fin y dispuestas sobre balanzas de precisión para saber en todo momento la cantidad de producto que están dosificando. En la situación ideal, cada tolva debería contener un único componente de la formulación y el propio sistema dosificaría de manera secuencial la cantidad de cada uno de los componentes, produciéndose la mezcla de manera adecuada en los primeros segmentos del granulador. En otros equipos, sin embargo, el sistema se alimenta de una única tolva en donde la mezcla homogénea se va dosificando. En este segundo caso y para poder ser considerado un equipo de producción en continuo, la mezcla debería proceder de una mezcladora en continuo. En cuanto a la alimentación del líquido para la granulación, es habitual emplear bombas peristálticas, aunque en caso necesario, es posible emplear otro tipo de bombas de mayor presión. En cuanto al volumen dosificado, se puede controlar mediante sencillos caudalímetros de Coriolis o mediante métodos gravimétricos.
En cuanto al secado de los gránulos recién formados, lo habitual es conectar el granulador mediante transporte neumático a lechos fluidos continuos como los comentados anteriormente. En el caso del sistema ConsiGma de GEA, el lecho fluido se encuentra segmentado en seis celdas independientes, es decir, subdivide en sublotes la producción continua de granulados para secarlos. El granulado húmedo accede a una de estas celdas mediante un distribuidor central, y el equipo va aportando aire caliente con un estado higrométrico bajo al principio, y frío y en equilibrio al final del ciclo, de tal manera que el gránulo seco es aspirado del equipo en unos pocos minutos y conducido a una unidad de caracterización. Existen algunos sistemas de secado a vacío asistido por microondas o por contacto, pero su uso industrial está todavía muy limitado.
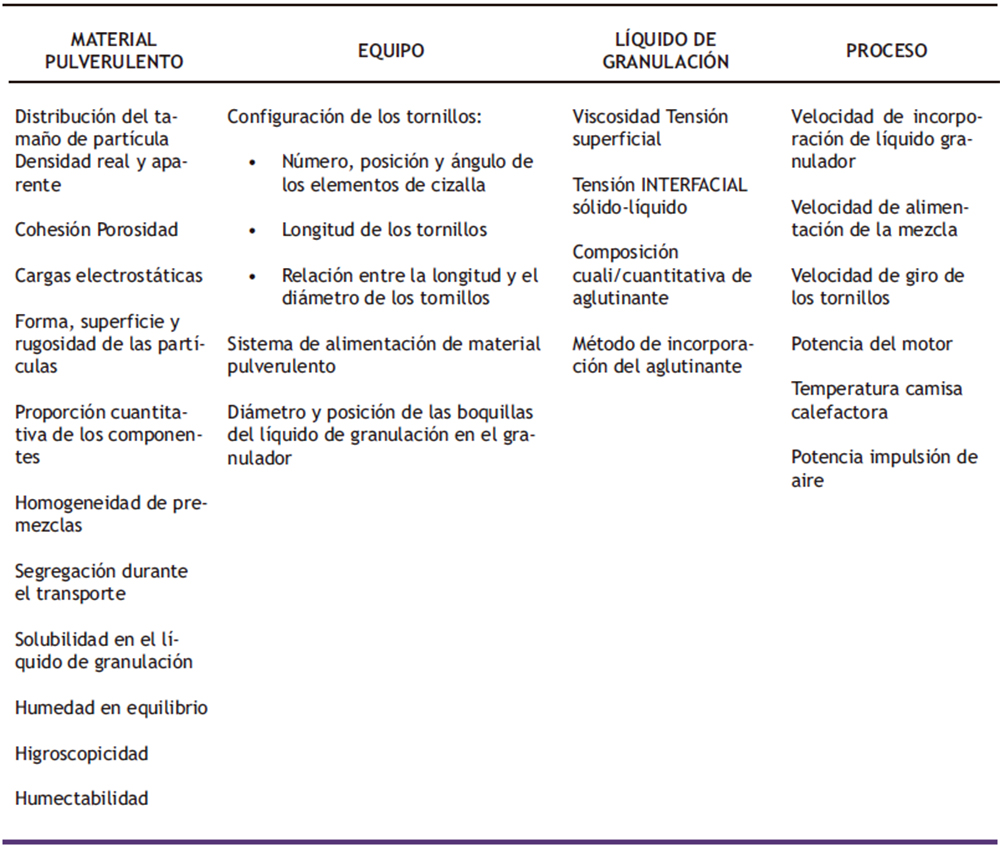
Los TSG son equipos que ofrecen un control superior sobre las características granulares en comparación con otras técnicas de granulación (45). Además, por su propio diseño aplican sobre la mezcla presiones y cizallas significativas, provocando que los gránulos obtenidos presenten una elevada densidad, debido fundamentalmente a la compresión de los puentes líquidos (46). Esto hace además que su capacidad para retener líquidos sea baja y por ende su estabilidad sea alta (47, 48). Las variables a considerar en la granulación húmeda mediante TSG aparecen recogidas en la tabla 1 (49, 50).
Tabla 1. Variables a considerar en la granulación húmeda mediante granuladores de tornillos gemelos
Las principales variables en este tipo de granuladores están relacionadas con la configuración de los tornillos. Existen segmentos de transporte de diferentes longitudes y diseños capaces de generar fuerzas rotacionales y axiales para mover la mezcla a lo largo del TSG sin compactarla o cortarla. Un aspecto importante de estos segmentos es la longitud de paso o distancia fija entre dos partes idénticas del segmento; un paso grande permite trasladar mayor cantidad de producto que un paso estrecho, por lo que se dispondrían en la zona de alimentación del tornillo. Sin embargo, un paso estrecho es más apropiado en zonas de mayor densificación del material (51). Por otro lado, el sistema incorpora segmentos de amasado y segmentos de corte o de alta cizalla, cuyo diseño, inclinación relativa frente al elemento contiguo (52), espesor (53), etc., hace que su capacidad de generar mezclas distributivas (aquellas que reducen la distancia física entre dos partículas para facilitar que se generen interacciones) y dispersivas (aquellas que rompen la fuerza de cohesión de aglomerados para facilitar cambios morfológicos y reducción de tamaño) en el proceso sea mayor (54, 55). Estos segmentos dependen del fabricante, no existiendo actualmente la posibilidad de intercambiarlos. Existen distintos estudios como el de El Hagrasy y colaboradores (56) que abordan la influencia de estas variables en la calidad final del granulado (57).
La relación sólido-líquido es un parámetro fundamental y específico de cada proceso. En general, la proporción de líquido mínima para conseguir gránulos es muy inferior a la necesaria en los sistemas tradicionales de lecho fluido o alta cizalla; esto facilita el secado posterior. Sin embargo, los gránulos obtenidos suelen presentar superficies irregulares y distribuciones bimodales con alta proporción de finos, que hacen indispensable una caracterización de los granulados como paso previo a su uso para compresión, lo que dificulta su integración en un sistema continuo. El incremento en la proporción de aglutinante en el líquido (58), o simplemente un incremento de líquido, permite conseguir distribuciones monomodales, pero habitualmente de tamaño excesivamente grande.
(59). Por último, es importante considerar que estos sistemas admiten una proporción de líquido mayor que los sistemas clásicos, llegando a la sobrehumectación y bloqueo del sistema si no se controlan adecuadamente el resto de las variables operacionales (60).
Otro aspecto relevante a considerar, al menos desde un punto de vista teórico, sería la velocidad de giro de los tornillos, ya que esta condicionaría la velocidad de alimentación y el tiempo de residencia de la mezcla en el sistema. En la práctica, numerosos estudios han demostrado que este aspecto no repercute de manera tan significativa en las propiedades de los gránulos elaborados, como la configuración del tornillo u otras variables del proceso, como la temperatura o la propia resistencia intrínseca del material (61, 62).
En una colaboración entre distintas universidades europeas y varias industrias farmacéuticas, se llevó a cabo un proceso de granulación húmeda y posterior compresión en una línea completa en continuo, empleando un TSG como granulador (Figura 2) (45). Como variables, se ensayaron la velocidad de alimentación de la mezcla, el número de elementos de corte y el ángulo relativo entre ellos, la temperatura de la camisa de recirculación y la manera de añadir la povidona K30, en húmedo o en seco. Como respuestas posibles se evaluaron el torque y la variación de temperatura del TSG, la distribución de tamaño de partícula por tamización analítica, la friabilidad y la fluidez del granulado obtenido y, por último, la resistencia a la fractura, porosidad, friabilidad, tiempo de disgregación y velocidad de disolución de la teofilina anhidra incorporada de los comprimidos. Los parámetros con mayor influencia en la calidad del granulado y de los comprimidos finales fueron el número de elementos de corte incorporados en los tornillos, no tanto su inclinación relativa, la manera de incorporar el aglutinante y la temperatura del cuerpo del granulador como consecuencia de las fricciones del material entre sí y con la pared interna del granulador. Equipos que carezcan de un sistema eficaz para mantener la temperatura del sistema no serían capaces de mantener el estado estacionario durante un tiempo prolongado en un proceso industrial a pesar del reducido tiempo de residencia.
Como continuación del estudio anterior, se incorporaron a la salida del TSG en línea una sonda Parsum® para determinar el tamaño de partícula de los gránulos recién obtenidos, una sonda Raman y una sonda NIR con transformada de Fourier, para evaluar la uniformidad y posibles variaciones de los espectros de la teofilina durante el proceso y determinar cuál sería la PAT más adecuada para este proceso (63). Como conclusiones de este estudio, se puso de manifiesto que ambas sondas eran adecuadas; si bien el Raman tenía mayor sensibilidad que el NIR. Durante el proceso y en función de las variables operacionales de las distintas pruebas realizadas, se demostró que si no se optimizaban estas de manera óptima, se podría generar teofilina monohidrato y formas metaestables que podrían modificar la eficacia terapéutica de la formulación final, en consonancia con estudios publicados con posterioridad (64).
Figura 2. Detalle de la línea ConsiGma 25 empleada en el estudio. A la izquierda se observa el lecho fluido de seis segmentos y a la derecha, conectado por vacío, el TSG equipado con una única tolva de alimentación de mezclas.
Recientemente, Fekete y cols. (65) han sido capaces de elaborar en continuo, comprimidos con granulación húmeda previa, empleando un TSG pero sin incorporar ningún líquido durante el proceso y evitando, por tanto, la necesidad de procesos de secado posteriores. Para ello, han calentado la mezcla durante la granulación, a la temperatura mínima para obtener el agua de cristalización del tartrato sódico incorporado a la mezcla. Si bien la velocidad de producción no es excesivamente alta y la técnica no es aplicable a principios activos termosensibles, la aproximación que han logrado supone un importante avance en la implantación de este tipo de técnicas.
En los últimos años, una vez conocida la influencia de las distintas variables en el proceso, existe un número significativo de publicaciones sobre modelado y simulación, como el modelado de balance poblacional, la dinámica de fluidos computacional, la técnica de elementos discretos y el software de modelado de procesos asociados a la generación de redes neuronales y a la inteligencia artificial, para comprender y optimizar procesos de granulación húmeda con TSG. A modo de ejemplo, Zahonyi y colaboradores (66) desarrollaron una red neuronal multicapa y una red neuronal antropomórfica a partir de los parámetros de proceso aplicados y sin necesidad de entrenarlas con mediciones analíticas directas. Una vez demostrada su capacidad predictiva, ajustaron la red multicapa para identificar los parámetros más influyentes y la emplearon como un sensor virtual a la autorregulación del proceso.
6. CONCLUSIONES
A raíz del avance regulatorio que ha supuesto la publicación de la guía ICH Q13 y de los distintos ejemplos de medicamentos autorizados, fabricados de forma continua, la fabricación en continuo es hoy día una realidad que promete abrir las puertas hacia una nueva filosofía de trabajo en la Industria Farmacéutica. La implantación de nuevas técnicas analíticas como RAMAN, NIR, etc., capaces de constituir sondas de tecnología analítica de procesos, merced a la posibilidad real de proporcionar datos de funcionamiento del sistema en tiempo real, así como las herramientas informáticas basadas en el Big Data y la Inteligencia Artificial, han hecho posible esta llamada cuarta revolución industrial o “Industria 4.0”.
En dicho contexto, la fabricación de medicamentos en diferentes formas farmacéuticas de forma continua es ya un hecho. La producción de comprimidos recubiertos en continuo ha demostrado su eficacia y su agilidad en comparación con los procedimientos “clásicos”, gracias a los nuevos equipamientos disponibles en el mercado industrial.
Sobre esta base, es difícil predecir la profundidad del impacto de esta nueva estrategia de fabricación que irrumpe con fuerza a nivel mundial, pero es seguro que la Industria Farmacéutica ha emprendido un camino de modernización, que supondrá una mayor agilidad en la producción de medicamentos, sin menoscabar sus estándares de calidad, seguridad y eficacia.
7. Referencias
- Vervaet C, Remon JP. Continuous granulation. In: Swarbrick J, Ed. Handbook of Pharmaceutical Granulation Technology. New York: Informa Healthcare; 2009; pp. 308-322.
- EU GMP Vol 4. Guidelines for Good Manufacturing Practices for Medicinal Products for Human and Veterinary Use. Pharmaceutical Quality System. Disponible en: https://health.ec.europa.eu/medicinal-products/eudralex/eudralex-volume-4_en [consultado noviembre 2025].
- Poli M, Quaglierini M, Zega A, Pardini S, Telleschi M, Iervasi G, Guiducci L. Risk Management in Good Manufacturing Practice (GMP) Radiopharmaceutical Preparations. Appl Sci 2024; 14(4): 1584.
- ICH Q10. Pharmaceutical Quality System – Scientific Guideline. 2015. Disponible en: https://www.ema.europa.eu/en/ich-q10-pharmaceutical-quality-system-scientific-guideline [consultado noviembre 2025].
- ICH Q9. Quality Risk Management – Scientific Guideline. 2015. Disponible en: https://www.ema.europa.eu/en/ich-q9-quality-risk-management-scientific-guideline [consultado noviembre 2025].
- Dixit S, Suryawanshi SJ, Arora S, Sharma N, Shukla VK. A Comprehensive Review on the Good Manufacturing Practices Standards. Understanding Pharmaceutical Standards and Regulations: Insights Towards Best Practice 2025; 2.
- https://health.ec.europa.eu/document/download/e99884fd-2b52-470b-9453-10346ddb6cbd_en
- Directiva 2001/83/CE del Parlamento Europeo y del Consejo, de 6 de noviembre de 2001, por la que se establece un código comunitario sobre medicamentos para uso humano. ELI: http://data.europa.eu/eli/dir/2001/83/oj
- Liu P, Jin H, Chen Y, Wang D, Yan H, Wu M, Zhu W. Process analytical technologies and self-optimization algorithms in automated pharmaceutical continuous manufacturing. Chin Chem Lett 2024; 35(3): 108877.
- García V, Córdoba M, Córdoba D, Garrosa M, Jiménez P, Girbés T. El reto de la fabricación en continuo en la industria farmacéutica. Pharmatech 2018; 37: 58-62.
- Nasr M, et al. Regulatory perspectives on continuous pharmaceutical manufacturing: moving from theory to practice: september 26–27, 2016, international symposium on the continuous manufacturing of pharmaceuticals. J Pharm Sci 2017; 106: 3199-3206.
- Yu LX, Kopcha M. The future of pharmaceutical quality and the path to get there. Int J Pharm 2017; 528: 354-359.
- Badman C, et al. Why we need continuous pharmaceutical manufacturing and how to make it happen. J Pharm Sci 2019; 108: 3521-3523.
- Pagliarulo N. Pharma’s slow embrace of continuous manufacturing. BiopharmaDive 2018. Disponible en: https://www.biopharmadive.com/news/pharmas-slow-embrace-of-continuous-manufacturing/532811/ [consultado noviembre 2025].
- Quality Considerations for Continuous Manufacturing; Draft Guidance for Industry. Docket No. FDA–2019–D–0298. Department of Health and Human Services – FDA. Federal Register 2019; 84(39).
- ASTM E2537-16. Standard Guide for Application of Continuous Process Verification to Pharmaceutical and Biopharmaceutical Manufacturing. ASTM International; 2016. Disponible en: https://store.astm.org/e2537-16.html [consultado noviembre 2025].
- ICH Q13. Continuous Manufacturing of Drug Substances and Drug Products. International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use; 2022.
- Arden NS, Fisher AC, Tyner K, Yu LX, Lee SL, Kopcha M. Industry 4.0 for pharmaceutical manufacturing: Preparing for the smart factories of the future. Int J Pharm 2021; 602: 120554.
- Morcillo-Bellido J, Merino-Fuentes R, Morcillo-García J. Industry 4.0: Impact Analysis on Global Pharma Companies’ Supply Chains. In: Internet of Things and Data Science in Engineering Management: Selected Papers from the 16th International Conference on Industrial Engineering and Industrial Management. Cham: Springer Nature Switzerland; 2025; pp. 53-64.
- Markarian J. Digitalization Moves Forward in Pharma Equipment and Processes. 2021.
- Kumar A, Sharad N, Kishore A. The synergy of artificial intelligence in life science operations and its impact on GDP. Int J DevOps 2024; 1(1): 27-40.
- Khanna A, El Barachi M, Jain S, Kumar M, Nayyar A, Eds. Artificial intelligence and machine learning in drug design and development. John Wiley & Sons; 2024.Singh S. Leveraging AI and Machine Learning in Six-Sigma Documentation for Pharmaceutical Quality Assurance. Chin J Appl Physiol 2024; 40: e20240005.
- Suriyaamporn P, Pamornpathomkul B, Patrojanasophon P, Ngawhirunpat T, Rojanarata T, Opanasopit P. The artificial intelligence-powered new era in pharmaceutical research and development: A review. AAPS PharmSciTech 2024; 25(6): 188.
- Vanhoorne V, Vervaet C. Recent progress in continuous manufacturing of oral solid dosage forms. Int J Pharm 2020; 579: 119194.
- Colón YM, Vargas J, Sánchez E, Navarro G, Romañach RJ. Assessment of robustness for a near-infrared concentration model for real-time release testing in a continuous manufacturing process. J Pharm Innov 2017; 12(1): 14-25.
- Beg S, Ahirwar K, Almalki WH, Almujri SS, Alhamyani A, Rahman M, Shukla R. Nondestructive techniques for pharmaceutical drug product characterization. Drug Discov Today 2025; 30(1): 104249.
- De Beer T, Burggraeve A, Fonteyne M, Saerens L, Remon JP, Vervaet C. Near infrared and Raman spectroscopy for the in-process monitoring of pharmaceutical production processes. Int J Pharm 2011; 417(1-2): 32-47.
- Galata DL, Peterfi O, Ficzere M, Szabó-Szőcs B, Szabo E, Nagy ZK. The current state-of-the art in pharmaceutical continuous film coating – A review. Int J Pharm 2025; 669: 125052.
- Alves-Lima D, Song J, Li X, Portieri A, Shen Y, Zeitler JA, Lin H. Review of terahertz pulsed imaging for pharmaceutical film coating analysis. Sensors 2020; 20(5): 1441.
- Wolfgang M, Poms J, Herndler V, Huegel I, Kipping T, Spoerk M, Khinast JG. Real-time monitoring of multiparticulate coating processes at industrial-scale using ultra-high-resolution optical coherence tomography. Int J Pharm 2025; 675: 125546.
- Péterfi O, Mészáros LA, Szabó-Szőcs B, Ficzere M, Sipos E, Farkas A, Nagy ZK. UV–VIS imaging-based investigation of API concentration fluctuation caused by the sticking behaviour of pharmaceutical powder blends. Int J Pharm 2024; 655: 124010.
- Ficzere M, Madarász L, Kádár S, Farkas A, Mészáros LA, Nagy ZK. UV imaging as a novel, ultrafast chemical mapping tool for pharmaceutical tablet analysis. Microchem J 2025; 115032.
- Péterfi O, Mészáros LA, Szabó-Szőcs B, Ficzere M, Sipos E, Farkas A, Nagy ZK. UV–VIS imaging-based investigation of API concentration fluctuation caused by the sticking behaviour of pharmaceutical powder blends. Int J Pharm 2024; 655: 124010.
- Liu P, Jin H, Chen Y, Wang D, Yan H, Wu M, Zhu W. Process analytical technologies and self-optimization algorithms in automated pharmaceutical continuous manufacturing. Chin Chem Lett 2024; 35(3): 108877.
- Adak S. Advances in the Synthesis and Optimization of Pharmaceutical APIs: Trends and Techniques. Univers J Pharm Pharmacol 2025; 4: 1239.
- Damiri H, Steinberger M, Kuchler L, Azimi A, Martinuzzi S, Sagmeister P, Horn M. Model-based real-time optimization in continuous pharmaceutical manufacturing. Comput Chem Eng 2025; 192: 108915.
- Roggo Y, Jelsch M, Heger P, Ensslin S, Krumme M. Deep learning for continuous manufacturing of pharmaceutical solid dosage form. Eur J Pharm Biopharm 2020; 153: 95-105.
- Colombo S. Applications of artificial intelligence in drug delivery and pharmaceutical development. In: Artificial Intelligence in Healthcare. Academic Press; 2020; pp. 85-116.
- Patel J, Patel D, Meshram D. Artificial intelligence in pharma industry – A rising concept. J Adv Pharmacogn 2021; 1(2): 54-64.
- Rajesh MV, Elumalai K. The transformative power of artificial intelligence in pharmaceutical manufacturing: Enhancing efficiency, product quality, and safety. J Holistic Integr Pharm 2025; 6(2): 125-135.
- Litster J, Ennis BJ. The Science & Engineering of Granulation Processes. Dordrecht: Kluwer Academic; 2004.
- Ennis BJ. Theory of Granulation: An Engineering Perspective. In: Parikh DM, Ed. Handbook of Pharmaceutical Granulation Technology. 2nd ed. Boca Raton: Taylor & Francis; 2005.
- Conti FB. Continuous Fluid Bed Agglomeration. NEUHAUS NEOTEC Maschinen- und Anlagenbau GmbH [Video]. YouTube; 2020. Disponible en: https://www.youtube.com/watch?v=vc8nvScFrMk [consultado noviembre 2025].
- Vercruysse J, Díaz DC, Peeters E, Fonteyne M, Delaet U, Van Assche I, et al. Continuous twin-screw granulation: Influence of process variables on granule and tablet quality. Eur J Pharm Biopharm 2012; 82: 205-211.
- Iveson SM, Litster JD, Hapgood K, Ennis BJ. Nucleation, growth and breakage phenomena in agitated wet granulation processes: A review. Powder Technol 2001; 117: 3-39.
- Peeters M, Jiménez AAB, Matsunami K, Ghijs M, dos Santos Schultz E, Roudgar M, et al. Analysis of the effect of formulation properties and process parameters on granule formation in twin-screw wet granulation. Int J Pharm 2024; 650: 123671.
- Dhenge RM, Cartwright JJ, Hounslow MJ, Salman AD. Twin-screw granulation: Steps in granule growth. Chem Eng J 2012; 164: 8.
- Meng W, Rao KS, Snee RD, Ramachandran R, Muzzio FJ. A comprehensive analysis and optimization of continuous twin-screw granulation processes via sequential experimentation strategy. Int J Pharm 2019; 556: 349-362.
- Kotamarthy L, Ramachandran R. Mechanistic understanding of the effects of process and design parameters on the mixing dynamics in continuous twin-screw granulation. Powder Technol 2021; 390: 73-85.
- Kitching VR, Rahmanian N, Jamaluddin NH, Kelly A. Influence of type of granulators on formation of seeded granules. Chem Eng Res Des 2020; 160: 154-161.
- Sarhangi Fard A, Anderson PD. Simulation of distributive mixing inside mixing elements of co-rotating twin-screw extruders. Comput Fluids 2013; 87: 79-91.
- Kittikunakorn N, Liu T, Zhang F. Twin-screw melt granulation: Current progress and challenges. Int J Pharm 2020; 588: 119670.
- Kittikunakorn N, Sun CC, Zhang F. Effect of screw profile and processing conditions on physical transformation and chemical degradation of gabapentin during twin-screw melt granulation. Eur J Pharm Sci 2019; 131: 243-253.
- Bravo VL, Hrymak AN, Wright JD. Numerical simulation of pressure and velocity profiles in kneading elements of a co-rotating twin-screw extruder. Polym Eng Sci 2000; 40: 525-541.
- El Hagrasy AS, Hennenkamp JR, Burke MD, Cartwright JJ, Litster JD. Twin-screw wet granulation: Influence of formulation parameters on granule properties and growth behavior. Powder Technol 2013; 238: 108-115.
- Alam A. Development of polymeric composites by using reactive melt blending process: A modern and advanced technology. Int J Adv Res 2018; 6: 478-483.
- Kotamarthy L, Dan A, Karkala S, Parvani S, Román-Ospino AD, Ramachandran R. Twin-screw granulation: Mechanistic understanding of the effect of material properties on key granule quality attributes through the analysis of mixing dynamics and granulation rate mechanisms. Adv Powder Technol 2023; 34: 104137.
- Verstraeten M, Van Hauwermeiren D, Lee K, Turnbull N, Wilsdon D, am Ende M, et al. In-depth experimental analysis of pharmaceutical twin-screw wet granulation in view of detailed process understanding. Int J Pharm 2017; 529: 678-693.
- Lee KT, Ingram A, Rowson NA. Comparison of granule properties produced using Twin-screw Extruder and High Shear Mixer: A step towards understanding the mechanism of twin-screw wet granulation. Powder Technol 2013; 238: 91-98.
- Vendola TA, Hancock BC. The effect of mill type on two dry-granulated placebo formulations. Pharm Technol 2008; 32: 72.
- Kittikunakorn N, Paul S, Koleng JJ, Liu T, Cook R, Yang F, et al. How Does the Dissimilarity of Screw Geometry Impact Twin-screw Melt Granulation? Eur J Pharm Sci 2021; 157: 105645.
- Fonteyne M, Vercruysse J, Díaz DC, Gildemyn D, Vervaet C, Remon JP, et al. Real-time assessment of critical quality attributes of a continuous granulation process. Pharm Dev Technol 2013; 18(1): 85-97.
- Zhang GG, Law D, Schmitt EA, Qiu Y. Phase transformation considerations during process development and manufacture of solid oral dosage forms. Adv Drug Deliv Rev 2004; 56(3): 371-390.
- Fekete D, Tóth RF, Nagy ZK, Cech T, Ries L, Szabó E. Continuous twin-screw wet granulation without addition of granulation liquid. Eur J Pharm Sci 2025; 107295.
- Záhonyi P, Fekete D, Szabó E, Nagy ZK, Nagy B. Explainable artificial neural network as a soft sensor to predict the moisture content in a continuous granulation line. Eur J Pharm Sci 2025; 212: 107173.