Page 5 - 81_01
P. 5
Carmen Avendaño
ÁcidoN-acetilmurámico CH2OH
O
N-acetilglucosamina CH2OH CH2OH O
O O
O H3C
O D-Ala O
H3C L-Ala
CH2OH O H3C CH2OH O O NHCOCH3
OH O NHCOCH3 OH L-Ala Glu-D
L-Ala
O O Glu-D L-Lys
Glu-D Pentapéptido
NHCOCH3 L-Lys (Gly)5 NH2 NHCOCH3 L-Lys (Gly)5 NH D-Ala
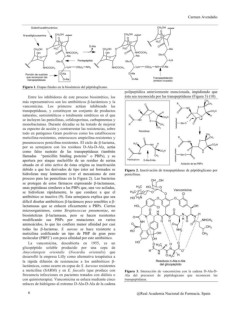
Porción de sustrato D-Ala D-Ala Transpeptidación
que reconocen las D-Ala D-Ala (enlace cruzado)
transpeptidasas
Figura 1. Etapas finales en la biosíntesis del péptidoglicano. polipeptídica anteriormente mencionada, impidiendo que
Entre los inhibidores de este proceso biosintético, los ésta sea reconocida por las transpeptidasas (Figura 3) (10).
más representativos son los antibióticos ß-lactámicos y la
vancomicina. Los primeros actúan inhibiendo las O CH3
transpeptidasas, y constituyen un conjunto de productos R CH3
naturales, semisintéticos o totalmente sintéticos en el que H NH
se incluyen las penicilinas, cefalosporinas, carbapenemas y NH S
monobactamas. Durante décadas se ha tratado de mejorar O CO2H O CO2H
su espectro de acción y contrarrestar las resistencias, sobre NH S
todo en patógenos Gram positivos como los estafilococos H NH
meticilina-resistentes, enterococos ampicilina-resistentes y R CH3
pneumococos penicilina-resistentes. El ciclo de ß-lactama, CH3 Ser-O O
por su semejanza con los residuos D-Ala-D-Ala, actúa
como falso sustrato de las transpeptidasas (también Penicilinas
llamadas “penicillin binding proteins” o PBPs), y su
apertura por ataque nucleófilo de un residuo de serina O R CH3
situado en el sitio activo de éstas origina su inactivación CH3
debido a que los derivados de tipo éster así formados se H3C NH H NH
hidrolizan muy lentamente (ver el mecanismo de este S
proceso para las penicilinas en la Figura 2). Las bacterias O CO2H O
se protegen de estos fármacos expresando ß-lactamasas, NH CH3 H CO2H
unas peptidasas similares a las PBPs que, una vez aciladas, D-Ala-D-Ala
se hidrolizan rápidamente, lo que conduce a que el Péptidoglicano NH
antibiótico se inactive (9). Esta semejanza explica que sea H
difícil diseñar antibióticos ß-lactámcos poco sensibles a ß-
lactamasas que se enlacen eficazmente a PBPs. Ciertos Ser-O
microorganismos, como Streptococcus pneumoniae, no
biosintetizan ß-lactamasas, pero se hacen resistentes O
modificando sus PBPs por mutaciones en varios
aminoácidos, lo que les confiere menor afinidad por casi Acilación de las PBPs
todas las ß-lactamas. S. aureus se hace resistente a
meticilina codificando un tipo de PBP de gran peso Figura 2. Inactivación de transpeptidasas de péptidoglicano por
molecular (PBP2’) con poca afinidad por este antibiótico. penicilinas.
La vancomicina, descubierta en 1955, es un OH OH
glicopéptido soluble producido por una cepa de
Amycolatopsis orientalis (Nocardia orientalis) que H3C HO O Vancomicina
desarrolló la empresa Lilly como alternativa terapéutica a Cl
la rápida difusión de resistencias a los antibióticos ß- H3C O O O
lactámicos, como ocurre en cepas de S. Aureous resistentes HO H2N O O
a meticilina (SARM) y en E. faecalis (que produce con
frecuencia infecciones en pacientes tratados con diálisis o HO Cl OH
con quimioterapia). Vancomicina se enlaza mediante cinco O H
enlaces de hidrógeno al extremo D-Ala-D-Ala de la cadena N O
ON
NH O NH
NN
O OH H
H O NHCH3
HO
OO CH3
NH2
CH3
OH
HO O H3C H H O
RN N O
H O H3C H
Residuos D-Ala-D-Ala
del glicopéptido
Figura 3. Interacción de vancomicina con la cadena D-Ala-D-
Ala del precursor de péptidogicano que reconocen las
transpeptidasas.
6 @Real Academia Nacional de Farmacia. Spain