1. INTRODUCCIÓN
Los genes, junto con los mecanismos que regulan su expresión y las posibles alteraciones que pueden sufrir, desempeñan un papel fundamental en la aparición y evolución de numerosas enfermedades. Estas alteraciones pueden manifestarse como trastornos monogénicos o mendelianos, desequilibrios cromosómicos, modificaciones epigenéticas u otros tipos de alteraciones complejas que afectan la expresión génica. El análisis genético, por su parte, tiene amplias aplicaciones en la prevención, el diagnóstico, el tratamiento y el pronóstico de enfermedades, así como en el seguimiento de los pacientes y en la investigación científica y clínica (1).
Existen varios tipos de pruebas genéticas (PG), cada una con una finalidad distinta (p. ej., cribado neonatal, pruebas de portadores, pruebas de diagnóstico prenatal, pruebas genéticas, pruebas genéticas predictivas y pruebas forenses) (2); entre ellas, la PG diagnóstica se utiliza para confirmar la enfermedad en un individuo sintomático; por otro lado, la PG predictiva identifica variaciones genéticas que aumentan el riesgo de una persona de desarrollar una enfermedad o afección clínica específica. La utilidad clínica de la PG depende de la evidencia obtenida sobre la contribución de la variante genética al diagnóstico, pronóstico o tratamiento de la enfermedad.
Cuando los rasgos y enfermedades son altamente heredables (es decir, rasgos y trastornos monogénicos determinados por una o pocas variantes), las pruebas genéticas serán precisas y muy predictivas. Por el contrario, cuando los rasgos y enfermedades solo están parcialmente influenciados por factores genéticos y la heredabilidad es baja, la capacidad predictiva de las pruebas que consideran solo una variante genética nunca será muy precisa. Es decir, en el caso de rasgos y enfermedades complejas, tener una variante genética no implica desarrollar un fenotipo determinado (3).
El avance tanto de la genética clínica como del desarrollo tecnológico ha permitido aplicar las técnicas genéticas en terapéutica, incluyendo la realización de estudios farmacogenéticos (identificación de la variabilidad de causa genética en la respuesta a fármacos); estudios de valor pronóstico de respuesta a terapias (como los perfiles genómicos o transcriptómicos o el análisis de la carga mutacional tumoral); las terapias enfocadas a diana molecular (fármacos dirigidos a alteraciones moleculares, también denominadas procesables o accionables) y, más recientemente, la terapia génica en humanos (basada en la edición génica) para tratar ciertas patologías.
Así, la información proporcionada por los estudios del genoma puede servir para predecir con mayor exactitud qué estrategias de prevención y tratamiento serán de mayor utilidad en grupos de personas específicos, lo que es un punto destacado en la medicina de precisión (4).
Las variaciones genéticas influyen en cómo los fármacos son procesados por el organismo y su análisis puede contribuir a incrementar la seguridad y la eficacia de los tratamientos. La variación génica entre individuos de una misma especie consiste en las pequeñas diferencias existentes en el ácido desoxirribonucleico (ADN) y contribuye a la evolución biológica y a la adaptación al medio, pero también a diferentes patologías. Esta variación génica puede repercutir en el fenotipo. Los polimorfismos de nucleótido único (SNP), también llamados polimorfismos de un solo nucleótido o polimorfismos de nucleótido simple, son el tipo de variación genética más común entre las personas. En promedio, ocurren una vez por cada 1000 nucleótidos, lo que significa que hay alrededor de 4 a 5 millones de SNP en el genoma de una persona. Para que una variante pueda ser clasificada como un SNP, se tiene que encontrar en al menos un 1% de la población. En este sentido, se han encontrado más de 600 millones de SNP en poblaciones alrededor del mundo.
Los genes que codifican transportadores o enzimas relacionadas con los procesos farmacocinéticos y farmacodinámicos pueden presentar variantes que pueden clasificarse en germinales (resultado de mutaciones que se transmiten a la descendencia) o somáticas (cuando se producen en células implicadas en el crecimiento de tejidos y órganos, y que no se transmiten a la descendencia). En términos generales, las variantes germinales ayudan a predecir la eficacia y la toxicidad de un fármaco, mientras que las variantes somáticas se utilizan para optimizar la elección del tratamiento y mejorar la efectividad.
Idealmente, el análisis de biomarcadores farmacogenómicos debería realizarse de forma previa a iniciar el tratamiento, aunque a veces se ha utilizado a posteriori para poder ajustar la farmacoterapia en casos refractarios o en los que se han producido reacciones adversas graves no esperables inicialmente. Además del análisis e informe farmacogenético (para los fármacos en los que exista evidencia de una interacción fármaco-gén relevante), es necesario emitir un informe farmacoterapéutico considerando el resto de medicación que pueda ser necesaria para el tratamiento del paciente. En ese sentido, es importante tener en cuenta que el resultado clínico de un fármaco puede cambiar respecto a lo que es esperable en relación con el estudio del genotipo debido a la interacción con otro fármaco. Por ello, hay que tener en cuenta también las interacciones farmacológicas, y prestar especial atención a aquellos fármacos que actúan como inductores o inhibidores de las enzimas que participan en los procesos de detoxificación hepática. En relación con esto, se define como fenoconversión al resultado de una interacción en la cual el fenotipo de un individuo cambia temporalmente respecto al esperado desde el genotipo debido a factores extrínsecos como otros fármacos, alimentos, factores ambientales, tabaquismo, etc.
A medida que avanza el campo de la genómica, las pruebas genéticas y genómicas son cada vez más comunes dentro y fuera del ámbito clínico. Las pruebas genéticas directas al consumidor (DTC) pueden definirse como cualquier prueba de ADN para un rasgo médico o no médico que se anuncia y vende directamente al público a través de Internet; la mayoría de estas pruebas genéticas no están reguladas, lo que significa que salen al mercado sin ningún análisis independiente para verificar las afirmaciones del vendedor. La insuficiencia de una reglamentación adecuada en el ámbito de las DTC, a nivel global, plantea desafíos adicionales y podría suponer una falta de protección para el usuario cuando estas pruebas se adquieren de forma directa sin la supervisión de un profesional sanitario que disponga de formación específica en genética clínica.
En ciertos casos es difícil distinguir una prueba de salud de una prueba de estilo de vida, lo que puede tener implicaciones importantes desde el punto de vista legal. Las pruebas genéticas y genómicas, al igual que otros tipos de pruebas diagnósticas, pueden evaluarse y regularse según los siguientes tres criterios (5):
Validez analítica: Se refiere a la capacidad de la prueba para predecir la presencia o ausencia de un gen o cambio genético en particular; es decir, si la prueba puede detectar de manera consistente y precisa si una variante genética específica está presente o ausente.
Validez clínica: Se refiere a la asociación de las variantes genéticas que se están analizando con la presencia, ausencia o riesgo de una enfermedad específica; es decir, si se ha demostrado de manera concluyente que tener una variante genética específica aumenta el riesgo o la probabilidad de tener una enfermedad o de desarrollar una enfermedad.
Utilidad clínica: Se refiere a si la prueba puede proporcionar información sobre el diagnóstico, el tratamiento, el manejo o la prevención de una enfermedad que será útil para los pacientes y los profesionales; es decir, si el uso de la prueba mejorará los resultados en salud.
El conocimiento genómico y sus técnicas de estudio han transformado profundamente la medicina del siglo XXI, orientándola no solo al tratamiento de las enfermedades, sino a su prevención, diagnóstico precoz y su tratamiento. En cuanto al enfoque terapéutico, la personalización de la medicina engloba tanto estrategias farmacogenéticas como el uso de otras terapias novedosas que incluyen, por ejemplo, las terapias avanzadas (terapia génica, terapia celular, ingeniería de tejidos y medicamentos combinados de terapia avanzada), cuyo uso está revolucionando la forma de abordar el tratamiento de enfermedades. Estas innovaciones plantean desafíos para el sistema sanitario en términos de acceso, regulación y sostenibilidad (6). Hasta la fecha, la aplicación de las pruebas genéticas con fines diagnósticos, predictivos y terapéuticos en la asistencia sanitaria ha ido en aumento.
2. FARMACOGENÓMICA: CONCEPTO Y GENERALIDADES
A priori, puede ser difícil predecir quién se beneficiará de un medicamento, quién no responderá y quién experimentará reacciones adversas. Las variantes en los genes que afectan la respuesta del organismo a los medicamentos pueden explicar, al menos en parte, las diferencias de respuesta al tratamiento y pueden ser utilizadas para predecir si un medicamento será efectivo para una persona en particular y qué dosis ayudará a prevenir reacciones adversas a medicamentos (RAMs).
La farmacogenética estudia el impacto de las variantes genéticas en la respuesta a los fármacos, mientras que la farmacogenómica amplía su alcance al estudiar las bases moleculares y genéticas de las personas, considerando tanto el ADN como el ácido ribonucleico (ARN), así como los productos de su expresión. Si bien es común que estos términos se empleen de forma indistinta, son conceptos diferentes. Así, la farmacogenética ofrece una herramienta de estratificación de la población, que permite elaborar estrategias preventivas y adaptar las estrategias terapéuticas en función de las características individuales de cada paciente (7).
Toda la información acerca de las variantes estudiadas se almacena en bases de datos de forma que puede consultarse la evidencia disponible sobre la funcionalidad de cada una de ellas. ClinPGx es una base de datos de acceso libre que recoge y anota toda la información en farmacogenética, como son publicaciones científicas, referencias a ensayos clínicos, información de las agencias reguladoras del medicamento, alelos, variantes, etc. (8).
Las agencias reguladoras recogen aquellos biomarcadores que se consideran suficientemente validados e incorporan su determinación, ya sea como recomendación u obligación en ficha técnica, para el uso en clínica de algunos medicamentos, contribuyendo a mejorar su seguridad y efectividad. Por ejemplo, en el caso de los antineoplásicos, desde 2020 la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) recomienda el genotipado del gen DPYD (dihidropirimidina deshidrogenasa), previo a la prescripción de fluoropirimidinas, para identificar en el paciente la presencia de variantes de actividad reducida o nula, evitando así casos de toxicidad grave. Por otra parte, la identificación de variantes del gen TPMT (tiopurina metiltransferasa) y NUDT15 (hidrolasa Nudix tipo 15), que codifican para enzimas responsables del metabolismo de mercaptopurina o tioguanina, permite adaptar la dosis para reducir el riesgo de mielosupresión.
La evidencia que apoya la utilidad clínica de las pruebas farmacogenéticas se está acumulando. Por ejemplo, el gran ensayo multicéntrico europeo PREemptive Pharmacogenomic testing for treating Adverse drug REactions (PREPARE) demostró una reducción del 30% en las reacciones adversas con pruebas farmacogenéticas. Swen et al. (9) realizaron este estudio de implementación cruzado, aleatorizado por grupos, controlado, multicéntrico, abierto, de un panel farmacogenético de 12 genes en 18 hospitales, nueve centros de salud comunitarios y 28 farmacias comunitarias en siete países europeos (Austria, Grecia, Italia, Países Bajos, Eslovenia, España y Reino Unido). Los participantes fueron genotipados para 50 variantes de línea germinal en 12 genes; aquellos participantes con una variante accionable, es decir, un resultado de prueba de interacción fármaco-gén para el cual el Dutch Pharmacogenetics Working Group (DPWG) recomendó un cambio de tratamiento farmacológico, fueron tratados de acuerdo con las recomendaciones del DPWG. Los pacientes del grupo control recibieron el tratamiento estándar. Se inscribió a 6944 pacientes y se les asignó para recibir tratamiento farmacológico guiado por genotipo o atención estándar. En los pacientes con un resultado de prueba de interacción fármaco-gén (n = 1558), se produjo una reacción adversa al medicamento clínicamente relevante en 152 (21,0%) de los 725 pacientes del grupo de estudio y en 231 (27,7%) de los 833 pacientes del grupo control, mientras que, para todos los pacientes, la incidencia fue de 628 (21,5%) de 2923 pacientes en el grupo de estudio y de 934 (28,6%) de 3270 pacientes en el grupo control. Por tanto, el tratamiento guiado por el genotipo mediante un panel farmacogenético de 12 genes redujo significativamente la incidencia de reacciones adversas a medicamentos clínicamente relevantes y fue factible en diversas organizaciones y entornos del sistema sanitario europeo.
En relación con la implantación de las pruebas farmacogenéticas, los principales desafíos se encuentran en la adecuada formación de los profesionales sanitarios y la puesta en marcha de equipos multidisciplinares que garanticen una comunicación fluida entre los distintos especialistas, la interpretación adecuada del informe con resultados genéticos y la financiación de las pruebas genéticas. La incorporación de nuevas pruebas de laboratorio debe ir acompañada de una adecuada validez analítica, validez clínica, utilidad clínica y valoración de los aspectos éticos, legales y sociales.
El desarrollo de marcadores genómicos relacionados con la respuesta al tratamiento es uno de los escenarios más prometedores de la farmacogenómica. Algunos biomarcadores de este tipo ya han sido aprobados por las agencias reguladoras como biomarcadores validados que exigen cambio en la ficha técnica del medicamento. Algunos ejemplos son el gen que codifica para el receptor del factor de crecimiento epidérmico (EGFR) o la expresión del gen HER2 entre otros marcadores tumorales (10).
Como se ha comentado previamente, las pruebas farmacogenómicas tienen el potencial de identificar pacientes con variantes genéticas que los ponen en riesgo de reacciones adversas a medicamentos y podrían mejorar la seguridad de los medicamentos y reducir las hospitalizaciones. A este respecto, un estudio realizado por Nunez-Torres et al. (11) que analizó 21 farmacogenes accionables en la población española reveló que el 98% de la población alberga al menos un alelo asociado a un cambio terapéutico y, por lo tanto, sería necesario un cambio terapéutico en una media de 3,31 de los 64 fármacos asociados.
3. RELEVANCIA DE LA VARIABILIDAD GENÉTICA EN LA RESPUESTA AL TRATAMIENTO FARMACOLÓGICO
Las variaciones individuales en la respuesta a fármacos son interacciones complejas, ya que diversos genes y el ambiente interactúan. Los factores que más influyen en la respuesta a los fármacos son la dosis administrada, la adherencia al tratamiento, la dieta, el consumo de alcohol y el tabaquismo; la propia enfermedad, particularmente enfermedades hepáticas y renales, puede afectar al metabolismo de los fármacos, al igual que las interacciones con otros fármacos.
En general, el fármaco se administra, se absorbe y distribuye hasta su lugar de acción, donde interactúa con su sustrato (habitualmente receptores y enzimas), se metaboliza y luego se excreta. Existen variaciones genéticas en cada una de estas etapas. El resultado varía de unos individuos a otros dentro de una población y esto afecta en mayor o menor medida a todos los fármacos.
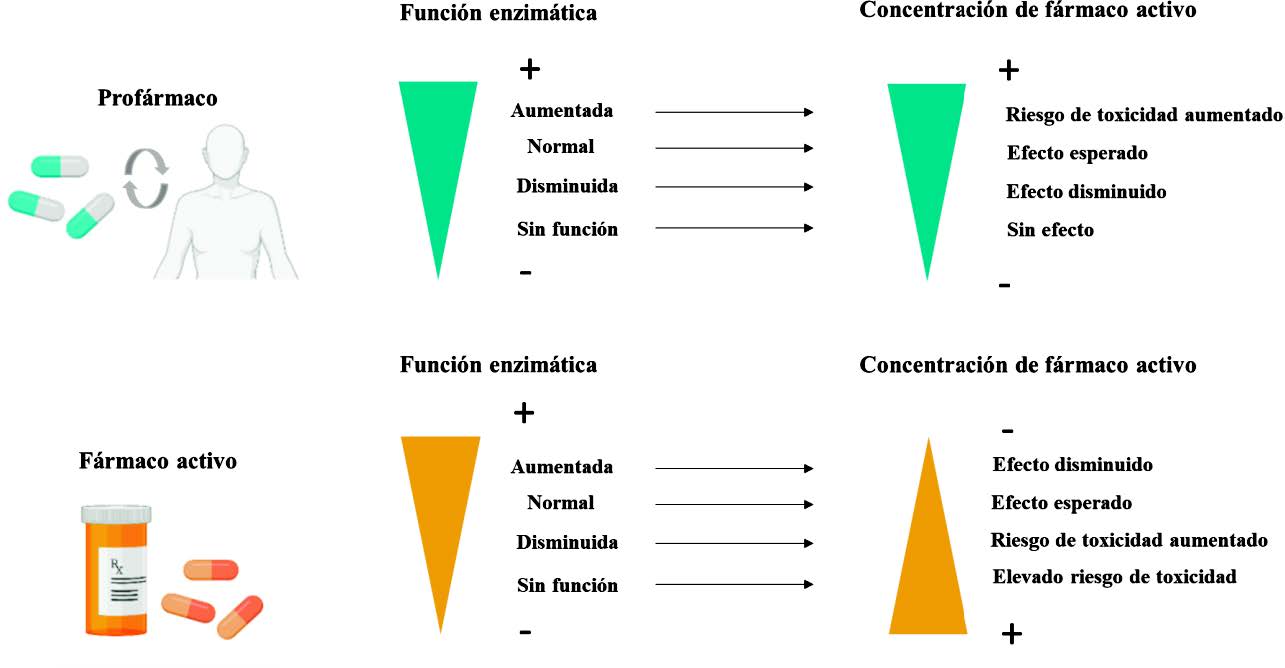
La investigación en farmacogenética ha dado lugar a un extenso conjunto de estas variantes que se consideran biomarcadores. A continuación, se describen algunos ejemplos de biomarcadores que inciden en la farmacocinética y la farmacodinámica. Las variantes farmacocinéticas, a su vez, pueden clasificarse según la funcionalidad para la que codifican, como variantes que codifican para alelos de función normal, disminuida, aumentada o sin función. La combinación de la funcionalidad de los alelos dará lugar a un fenotipo metabolizador (normal, intermedio, lento y ultrarrápido), que tendrá distintas consecuencias según la relación entre la función enzimática y la concentración de fármaco activo (con variantes anómalas se observan efectos opuestos según se trate de un fármaco activo o un profármaco) (12). Ver figura 1.
Figura 1. Variabilidad en la respuesta a fármacos. La variabilidad en la respuesta a fármacos puede estar condicionada por variantes genéticas en las enzimas encargadas de metabolizar fármacos o activar profármacos, lo cual influye en las concentraciones plasmáticas del principio activo. Adaptada de (12). Imagen creada con BioRender.com.
3.1. Biomarcadores que inciden en la farmacocinética
Los genes involucrados en los procesos farmacocinéticos se clasifican generalmente en tres categorías (13):
Reacciones de metabolización enzimática de fase I y II, responsables de los procesos de modificación de grupos funcionales y conjugación respectivamente (como pueden ser los genes de las familias CYP y UDP-glucuroniltransferasas).
Proteínas transportadoras, responsables de la absorción y excreción de fármacos dentro y fuera de la célula (como pueden ser la familia de los transportadores ATP binding-cassette y SLCO1B1, polipéptido transportador de aniones orgánicos 1B1).
Modificadores y factores de transcripción que pueden alterar la expresión de los genes de los procesos farmacocinéticos o afectar a la bioquímica de las enzimas de los procesos farmacocinéticos, como por ejemplo el citocromo P450 oxidoreductasa.
De las enzimas metabolizadoras de fármacos, las más importantes son las integradas en la superfamilia del citocromo P450, que actúa en el metabolismo de aproximadamente el 25-30% de los fármacos (incluyendo la práctica totalidad de los antidepresivos, antipsicóticos, anticonvulsivantes y anticoagulantes).
CYP2D6
Los polimorfismos y haplotipos del CYP2D6 varían considerablemente entre poblaciones humanas, lo que podría explicar algunas diferencias poblacionales en la respuesta a fármacos metabolizados por esta enzima. Entre estos fármacos podemos destacar los antiarrítmicos, antidepresivos, betabloqueantes, neurolépticos y otros como la codeína y el tamoxifeno. Entre las primeras pruebas farmacogenéticas aprobadas en los Estados Unidos (EE.UU.) para su uso en el entorno clínico cabe mencionar el análisis del CYP2D6.
CYP2C19
Son sustratos de estas enzimas los fármacos anticonvulsivantes como la fenitoína; los inhibidores de la bomba de protones como el omeprazol; los anticoagulantes; benzodiacepinas como el diazepam; barbituratos; antidepresivos como el citalopram.
CYP3A5
La familia 3A del complejo de los citocromos P450 está implicada en el metabolismo de un gran porcentaje de fármacos, entre ellos el prasugrel. Cataliza reacciones de oxidación, peroxidación y reducción.
N-acetiltransferasa tipo 2 (NAT2)
La acetilación es una de las rutas metabólicas más activas en la degradación de xenobióticos. Varios alelos del gen NAT2 se traducen en una enzima de baja actividad, dividiendo a la población en acetiladores rápidos y lentos de fármacos como isoniacida, hidralazina, dapsona, sulfamidas, dipirona y cafeína. En africanos subsaharianos y población caucásica de Europa y Norteamérica hay alrededor de 70% de acetiladores lentos, mientras en las poblaciones asiáticas solo entre 10% y 30%. Las poblaciones americanas aparecen en un lugar intermedio entre europeos/africanos y asiáticos con 60% de acetiladores lentos. Aunque no se han establecido de forma concluyente las consecuencias clínicas del fenotipo acetilador en el metabolismo de fármacos, sí se ha asociado el fenotipo acetilador lento con mayor riesgo de neuropatía por isoniacida, de síndrome lúpico inducido por hidralazina y de reacciones tóxicas provocadas por sulfamidas entre otras.
Metiltransferasas
La tiopurina metiltransferasa es una enzima genéticamente polimórfica, cataliza la metilación de los fármacos del grupo de las tiopurinas (azatioprina, mercaptopurina y tioguanina). La actividad de TPMT varía entre diferentes grupos poblacionales, y la farmacogenética de la TPMT representa uno de los mejores ejemplos del potencial de implicaciones clínicas del polimorfismo genético de una enzima metabolizadora de fármacos.
3.2. Biomarcadores que inciden en la farmacodinámica
La información sobre los factores genéticos que afectan el metabolismo y el transporte de fármacos excede en mucho la de los factores que inciden sobre la respuesta. La identificación de los genes y los polimorfismos implicados en los fenotipos de respuesta a fármacos es una labor más ardua, pues la búsqueda con frecuencia debe incluir no solo las dianas del fármaco y las que están implicadas en los eventos posreceptor, sino otras vías relacionadas. Algunos de este tipo de biomarcadores se están encontrando mediante estudios de asociación con SNPs que cubren todo el genoma.
Un ejemplo es la Vitamina K epóxido reductasa (VKOR). La warfarina inhibe esta enzima, codificada por el gen VKORC1, y de esa forma impide la activación de los factores de la coagulación II, VII, IX y X, que dependen de la vitamina K reducida. En las dosis efectivas individuales de warfarina inciden factores genéticos relacionados con los polimorfismos, tanto del gen VKORC1 como del gen que codifica la enzima CYP2C9.
Además, las variantes en el complejo mayor de histocompatibilidad explican algunas diferencias de reacciones de hipersensibilidad a fármacos.
4. TRASLACIÓN DE LA FARMACOGENÉTICA A LA PRÁCTICA CLÍNICA
En la era de la medicina de precisión, la farmacogenética tiene un potencial sustancial para abordar la variabilidad interindividual en las respuestas a los medicamentos.
La farmacogenética se está aplicando en hospitales para optimizar el tratamiento farmacológico en las enfermedades autoinmunes, en trasplantes de órgano sólido, infecciones por el virus de la inmunodeficiencia humana (VIH), tumores sólidos y hematológicos, enfermedades cardiovasculares y enfermedades psiquiátricas. Además de haber contribuido a los avances en el tratamiento personalizado en las áreas de oncología, psiquiatría, neurología, cardiología y medicina interna, es previsible que se extienda al resto de áreas conforme avance el conocimiento científico a partir de los numerosos estudios que se están desarrollando en todo el mundo.
En la actualidad, no existe un marco regulatorio que imponga una homogeneidad para las pruebas farmacogenéticas y parece obvio que un marco legal adecuado podría favorecer la implementación clínica de la farmacogenética. En cualquier caso, los grupos científicos han sido más ágiles al respecto que las agencias reguladoras. Así, cabe destacar las guías de Pharmacogenomics Knowledge Base (PharmGKB, actualmente integradas en ClinPGx) que han facilitado la organización y el acceso a la información científica disponible en farmacogenética, y se han establecido consorcios para coordinar la investigación y la traslación a la práctica clínica.
La farmacogenética es un campo en continuo crecimiento y es una realidad solo para un número reducido de fármacos. Se conocen centenares de biomarcadores que posiblemente influyan en la respuesta a fármacos, sin embargo, no todos disponen de la suficiente evidencia y, por tanto, se siguen realizando estudios para su validación.
Además, hay que tener en cuenta que no todos los biomarcadores validados se consideran obligatorios, y que existen diferencias en los biomarcadores aprobados por la Agencia Europea de Medicamentos (EMA) y otras agencias reguladoras como la Administración de Alimentos y Medicamentos de Estados Unidos (FDA).
Incluso en aquellos casos en los que el uso clínico es obligado o altamente recomendable, la implantación no es completa en todos los centros clínicos.
Las pruebas farmacogenéticas se han incorporado en algunos entornos de práctica clínica; en la mayoría de los países, la implementación sigue estando limitada a varias combinaciones de genes y fármacos (14). En este sentido, cabe destacar que existe un consenso general entre los miembros del Grupo de Trabajo de Implementación de la Red Global de Investigación en Farmacogenómica de que la información genética, al igual que la función renal o la consideración de las interacciones medicamentosas, puede servir para optimizar la terapia de forma individualizada y, de manera similar a la función renal o la consideración de las interacciones medicamento-medicamento, no requiere evidencia de ensayos clínicos de su utilidad antes de la implementación, en particular cuando los resultados de las pruebas genéticas ya están disponibles (15).
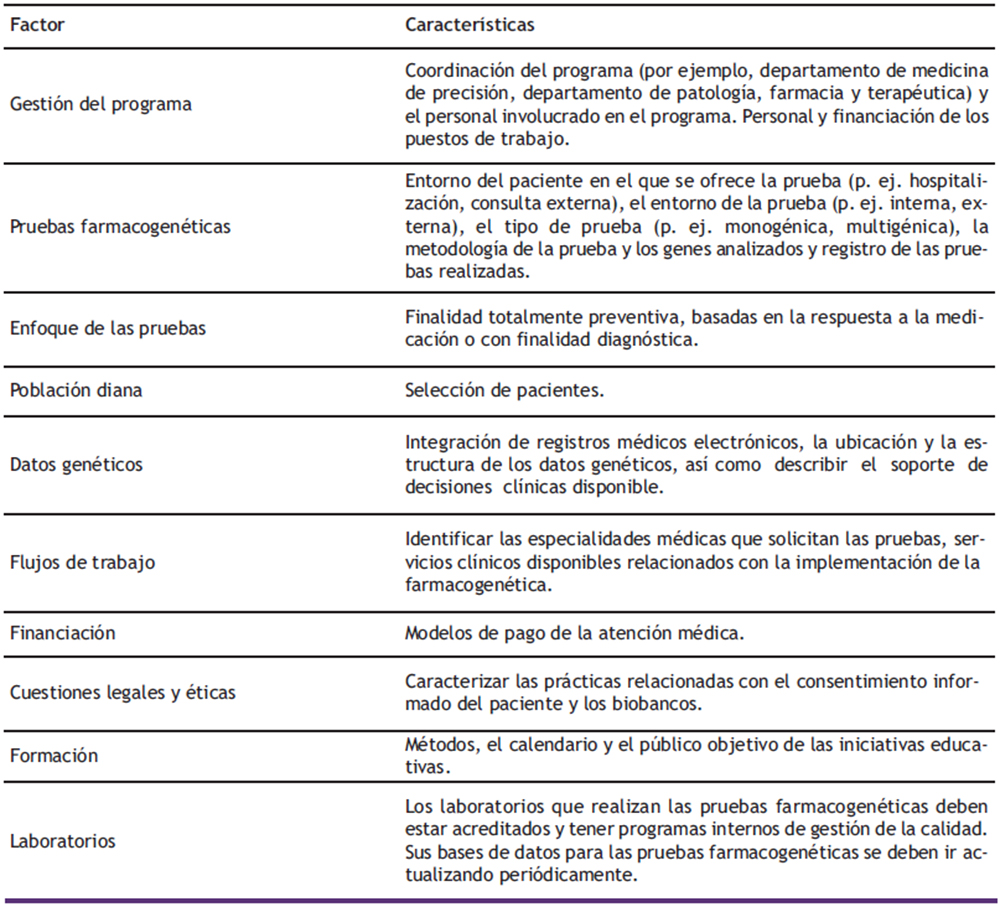
Una de las claves de la traslación a la clínica ha sido la mejoría notable de la tecnología de análisis y la disminución de su coste. El hecho de que se disponga en la actualidad de mayores conocimientos, unido al avance tecnológico, permite poder efectuar este tipo de pruebas con fiabilidad, alta sensibilidad y especificidad, lo que es fundamental para realizar un análisis poco costoso en un período de tiempo tal que no supone un retraso excesivo para el inicio del tratamiento. Los factores generales a considerar en las prácticas de implementación se describen en la Tabla 1.
Tabla 1. Factores que influyen en la implementación de la farmacogenética en la práctica clínica. Tabla adaptada de (15).
Existen diferentes barreras y oportunidades para la implementación generalizada de las pruebas farmacogenéticas en la práctica clínica. Entre las barreras cabe señalar los costes, desafíos técnicos en el genotipado y la falta de formación especializada de los profesionales, además de los escasos estudios sobre cómo integrar con éxito las pruebas en los flujos de trabajo clínicos y la escasez de datos sobre los resultados de la implementación farmacogenética en la práctica clínica. En este sentido, existen grupos de trabajo internacionales como el Grupo de Trabajo de Implementación de la Red Global de Investigación en Farmacogenómica que buscan involucrar a instituciones de todo el mundo con el fin de implementar las pruebas farmacogenéticas en la práctica clínica y difundir colectivamente datos sobre estrategias de implementación, métricas y resultados relacionados con la salud mediante el uso de la farmacoterapia guiada por el genotipo (15). Entre las oportunidades, cabe señalar el impacto transformador de la inteligencia artificial, mediante los algoritmos de aprendizaje automático y aprendizaje profundo, para abordar la complejidad de datos genómicos que implica la medicina personalizada (16).
Cabe señalar además que los países tienen diferentes umbrales de relación coste-efectividad, diferentes modelos de pago para los servicios de salud, diferentes costes para medicamentos y servicios, y diferentes frecuencias de las variantes farmacogenéticas según la etnia. Por lo tanto, la relación coste-efectividad en un país puede no traducirse directamente en relación coste-efectividad en otro.
Entre los estudios realizados, se puede mencionar un análisis sobre el coste-efectividad de las pruebas farmacogenéticas de forma previa a la prescripción, siguiendo las directrices del Consorcio de Implementación de Farmacogenética Clínica. Así, una revisión sistemática con estudios de alta calidad indicó una relación favorable coste-efectividad de las pruebas farmacogenéticas; si bien existen datos limitados sobre la relación coste-efectividad de las pruebas preventivas y multigénicas en los diferentes estados de la enfermedad (17).
De forma similar, en una revisión sistemática previa elaborada por Plöthner et al. (18), se analizó la relación coste-efectividad y coste-utilidad de pruebas farmacogenéticas. En la mayoría de los estudios incluidos, se informó que un tratamiento guiado por pruebas farmacogenéticas era coste-efectivo o conduciría a ahorros de costes. Los autores señalan que la relación coste-efectividad depende de varios factores, incluyendo la sensibilidad y especificidad de los procedimientos analíticos, la prevalencia de biomarcadores, los costes de las pruebas, la prevalencia de RAMs, la tasa de respuesta de la terapia, entre otras. También encontraron diferencias en la relación coste-efectividad incluso dentro de las mismas indicaciones.
Hay que considerar que los potenciales beneficios de las pruebas farmacogenéticas solo se pueden lograr si los facultativos realizan los cambios de medicación impulsados por los resultados de las pruebas farmacogenéticas. Así, estudios que han examinado la evidencia sobre el impacto de las pruebas farmacogenéticas en los cambios de medicación muestran que los cambios de medicación ocurrieron significativamente con mayor frecuencia en el tratamiento guiado por genotipo que en el tratamiento habitual. Además, los estudios también subrayan que hay que tener en cuenta cómo las perspectivas de los pacientes influyen en la adherencia a la farmacoterapia y en cómo toman sus medicamentos; en consecuencia, también es necesario investigar la actitud de los pacientes en relación con los tratamientos instaurados en base a pruebas farmacogenéticas (19).
Adaptar el tratamiento al genotipo del paciente ha demostrado ser eficaz para diversos pares fármaco-gén, reduciendo los eventos adversos y aumentando la eficacia. Sin embargo, existen diferencias significativas entre las recomendaciones de los Consorcios Farmacogenéticos y los posicionamientos de sociedades científicas relevantes. Existen diversas guías y recomendaciones disponibles de los principales Consorcios de Farmacogenética como el Clinical Pharmacogenetics Implementation Consortium (CPIC), DPWG, Réseau national de pharmacogénétique y Red Canadiense de Farmacogenómica para la Seguridad de los Medicamentos sobre cómo aplicar los resultados farmacogenéticos para optimizar la farmacoterapia. Actualmente, los expertos en Europa demandan alcanzar un consenso más amplio y que se emitan recomendaciones oficiales sobre cómo ajustar el tratamiento según el perfil genético del paciente, a poder ser desde los órganos de decisión y regulatorios como la EMA.
Por ejemplo, en el marco del cuidado de pacientes diagnosticados con cáncer para guiar la terapia con fluoropirimidinas e irinotecán, la implementación de DPYD y UGT1A1 (uridina difosfato glucuronosiltransferasa 1A1) es una estrategia para mitigar las toxicidades inducidas por fármacos. Y si bien la EMA recomienda realizar pruebas para la deficiencia de DPYD antes de iniciar la terapia con fluoropirimidinas, la National Comprehensive Cancer Network no lo hace.
Organizaciones profesionales como el CPIC, DPWG y la Red Canadiense de Farmacogenómica para la Seguridad de los Medicamentos sintetizan los datos disponibles para producir pautas basadas en la evidencia diseñadas para que los médicos traduzcan los resultados de las pruebas genéticas en decisiones de prescripción. A mediados de 2024, el CPIC publicó 26 directrices, cada una centrada en un fármaco o clase de fármaco único para el que se ha demostrado una interacción farmacogenética significativa. Otras organizaciones como Standardizing Laboratory Practices in Pharmacogenomics y la Asociación de Patología Molecular Americana, trabajan para armonizar los estándares, prácticas y recursos de las pruebas farmacogenéticas (15).
Las directrices CPIC para clopidogrel y tiopurinas fueron las primeras en publicarse, lo que refleja el alto grado de evidencia que respalda el uso guiado por genotipo de estos medicamentos y, por lo tanto, no es sorprendente que se encuentren entre los ejemplos más comunes de implementación farmacogenética.
También se han publicado documentos de posicionamiento conjunto; entre ellos, se pueden destacar las recomendaciones de genotipado de TPMT y NUDT15 de la Asociación de Patología Molecular Americana, el CPIC, el Colegio de Patólogos Estadounidenses, el DPWG de la Real Asociación de Farmacéuticos Holandeses, la Sociedad Europea de Farmacogenómica y Terapia Personalizada y PharmGKB (20).
La implementación de la farmacogenética en la práctica clínica se ha desarrollado fundamentalmente en hospitales públicos y privados. En los hospitales se han constituido comités multidisciplinares que se reúnen de forma periódica y en la mayoría de ellos se requiere una estrecha coordinación entre diversos servicios, entre los cuales cabe mencionar farmacia hospitalaria y análisis clínicos. La aplicación de pruebas farmacogenéticas a pacientes ambulatorios en la farmacia comunitaria y centros de salud se ha descrito fundamentalmente dentro del ámbito de la investigación (9, 21).
De acuerdo con una encuesta realizada por la Sociedad Española de Farmacia Hospitalaria en 2024, más de la mitad de los hospitales españoles realizan actividades de farmacogenética, con avances en la implementación del Catálogo Común de Servicios del Sistema Nacional de Salud (SNS) de Farmacogenómica. En el 60% de los hospitales, los especialistas en farmacia hospitalaria realizan la recomendación farmacoterapéutica tras la determinación genética. De esta encuesta se deriva también que, en relación con la farmacogenética, la farmacia hospitalaria participa en actividades de investigación, formación, protocolización y selección de medicamentos en comités de tumor molecular o desarrollo de alertas en sistemas de información clínica. Esto puede atribuirse, en parte, a que el servicio de farmacia de un hospital constituye el punto de unión entre los diferentes servicios clínicos para la realización de las recomendaciones farmacoterapéuticas que permiten la personalización del tratamiento basado en pruebas genéticas y, además, dispone de los conocimientos en cinética, logrando de esta forma una integración de las herramientas disponibles para la individualización de los tratamientos (22).
En los hospitales españoles, la determinación genética se lleva a cabo mayoritariamente en los servicios de genética o el servicio de análisis clínicos y, en menor medida, la realiza un laboratorio externo. La mayoría de los informes son emitidos por servicios de genética o análisis clínicos, y las recomendaciones farmacoterapéuticas son principalmente realizadas por farmacéuticos hospitalarios, si bien en ocasiones las realiza el médico responsable del paciente, biólogo genetista o farmacólogo clínico.
La colaboración interdisciplinar y la formación continua son elementos esenciales para superar los retos actuales y consolidar unidades funcionales de farmacogenética para que se desarrolle la farmacogenética como un estándar asistencial en los servicios de salud y avanzar hacia un modelo de medicina más precisa y efectiva.
Para comprender mejor el panorama global de la implementación de programas de farmacogenética y las estrategias exitosas para integrar la genotipificación en la atención al paciente, el Grupo de Trabajo de Implementación de la Red Global de Investigación en Farmacogenómica (15) realizó, a principios de 2024, una encuesta entre sus miembros, un total de 54 instituciones; el objetivo era evaluar las características institucionales, las implementaciones farmacogenéticas en ese momento y las que se estaban planificando. De las 39 instituciones que respondieron a la encuesta, el 79% era de los EE. UU., mientras que el resto eran de otros países. Entre los resultados obtenidos, el 90% de las instituciones que respondieron habían implementado clínicamente pruebas farmacogenéticas. La estrategia de implementación inicial informada en cada sitio ilustró un cambio de pruebas de un solo gen a pruebas de múltiples genes en los últimos años. Los diferentes pares gen-fármaco más implementados fueron: CYP2C19-clopidogrel, TPMT/NUDT15-tiopurinas, CYP2C19/CYP2D6-antidepresivos, CYP2D6-opioides, CYP2C19-voriconazol y CYP3A5-tacrolimus. Los medicamentos antipsicóticos CYP2D6 más comunes implementados fueron aripiprazol, brexpiprazol, haloperidol y risperidona. Entre la asociación del CYP2D6 y los inhibidores de la recaptación de serotonina, el más implementado fue venlafaxina. Casi todos los sitios (el 92%) informaron haber usado las pautas del CPIC para informar qué pares gen-fármaco incluir para la implementación; el 79% usó la guía de la FDA, el 68% usó la guía de la Asociación de Patología Molecular Americana, el 58% usó las pautas del DPWG y el 13% usó las pautas de práctica clínica de las sociedades médicas.
Carter et al. (23) realizaron un análisis sobre la implementación de la farmacogenómica en el contexto del Servicio Nacional de Salud de Inglaterra (NHS) identificando los posibles desafíos y sugiriendo recomendaciones específicas sobre el sistema de notificaciones electrónicas en relación con información farmacogenómica en el ámbito clínico que puede facilitar el proceso de prescripción y dispensación del medicamento. Entre los desafíos detectados en el NHS, extrapolables a otros sistemas de salud financiados con fondos públicos, se encuentran: precaución en el uso de alertas para evitar la fatiga; establecer análisis iterativos; necesidad de gobernanza del sistema, con supervisión y responsabilidad clínica; educación y formación continuada para profesionales y pacientes e identificar las consideraciones específicas para cada paciente.
La colaboración entre centros que han implementado con éxito el mismo par gen-fármaco y grupos de trabajo internacionales permitirá compartir datos para crear una población de pacientes lo suficientemente amplia para examinar los resultados de la implementación farmacogenética. Además, abrirá vías de colaboración, en particular para abordar poblaciones subrepresentadas, alelos raros y resultados poco frecuentes que requieren cohortes grandes (15).
5. DETERMINACIONES FARMACOGENÉTICAS, INTERPRETACIÓN Y REQUISITOS DE CALIDAD
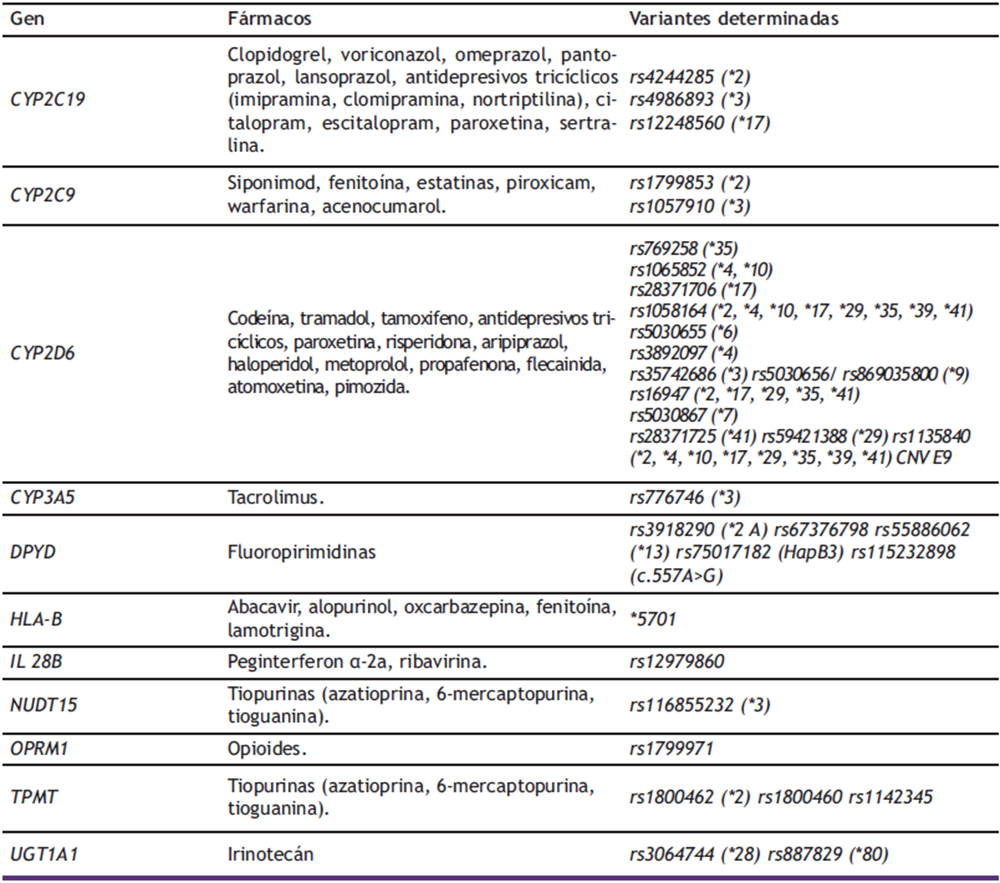
Las consideraciones a tener en cuenta sobre las pruebas farmacogenéticas clínicas se exponen a continuación. Las pruebas farmacogenéticas clínicas son particularmente valiosas cuando están respaldadas por evidencia científica sólida y relevancia clínica demostrada, y cuando los resultados pueden guiar la selección de medicamentos alternativos o ajustes de dosis (24). La presencia de guías estandarizadas mejora aún más su usabilidad como herramienta clínica. En la Tabla 2 se pueden consultar algunas asociaciones gen-fármaco clínicamente relevantes.
Tabla 1. Asociaciones gen-fármaco clínicamente relevantes. Tabla adaptada de (24).
Las pruebas farmacogenéticas se pueden realizar de forma retrospectiva para identificar predisposiciones genéticas en pacientes que han mostrado reacciones adversas a los tratamientos farmacológicos convencionales o de forma prospectiva para predecir las respuestas terapéuticas y los efectos secundarios antes de iniciar el tratamiento, lo que permite una dosificación segura y eficaz.
Los resultados de las pruebas de laboratorio clínico deben ser apropiados, precisos y confiables. Sin embargo, varios factores, que van desde errores sistemáticos o aleatorios hasta errores administrativos en el genotipado o la interpretación, pueden comprometer la calidad de los resultados, lo que puede poner en riesgo a los pacientes. Por lo tanto, la gestión de riesgos es esencial en cada etapa. Los genotipos son inherentes y permanecen inalterados a lo largo de la vida. Por ello, un error en las pruebas puede llevar a una mala interpretación de los resultados de por vida. Además, la interpretación incorrecta y los ajustes de dosis pueden aumentar los riesgos de toxicidad y fracaso del tratamiento. Como consecuencia, los laboratorios clínicos deben implementar planes de mejora de la calidad para mitigar los riesgos potenciales y garantizar la aplicación segura y eficaz de las pruebas farmacogenéticas en la práctica clínica.
Según la actualización de las guías de farmacogenética de la Sociedad Coreana de Medicina de Laboratorio, se exponen a continuación los requisitos de las pruebas farmacogenéticas clínicas (14):
- El grado de correlación entre las variantes genéticas y los resultados de la respuesta a los fármacos (poder predictivo de la respuesta a fármacos) debe estar bien establecido.
- Debe haber evidencia clara y suficiente que respalde la utilidad clínica de las pruebas farmacogenéticas, como estudios a gran escala, ensayos controlados aleatorizados y metaanálisis.
- Debe haber directrices claras y estandarizadas sobre cómo utilizar la información farmacogenómica para seleccionar los fármacos y ajustar las dosis.
- Debe disponerse de información sobre los tipos y la distribución de alelos y genotipos en los diferentes grupos étnicos o raciales.
- Se debe tener en cuenta también la viabilidad técnica y la capacidad analítica de los métodos de ensayo, así como la facilidad de uso, el rendimiento analítico esperado y el coste de las pruebas.
- Necesidad de proporcionar una interpretación exhaustiva de los resultados respaldada por el conocimiento y la experiencia adecuados en diversos campos, como la medicina, la farmacología clínica, la genética clínica y el laboratorio clínico.
- El tiempo necesario para obtener los resultados de las pruebas debe ajustarse a las indicaciones clínicas y a los requisitos del entorno sanitario.
- La utilidad clínica de la prueba debe justificar su coste, con un equilibrio favorable entre los gastos de la prueba y los beneficios obtenidos.
Además, al interpretar los resultados del genotipado, es esencial tener en cuenta factores como la edad, el peso, el estado de la enfermedad, el historial detallado de medicación y los fármacos coadministrados, los hallazgos de otras pruebas, las concentraciones de fármacos o metabolitos, las respuestas clínicas y los efectos secundarios. Este enfoque integral ayuda a determinar el fármaco y la dosis más adecuados para cada paciente.
El informe de la prueba debe diseñarse cuidadosamente para comunicar eficazmente los resultados de la prueba farmacogenética a los médicos. El informe debe explicar claramente los resultados y minimizar el uso de jerga especializada o técnica para facilitar una comunicación fluida entre los especialistas de laboratorio y los clínicos. El informe final debe incluir un resumen de la interpretación de los resultados de la prueba, junto con un análisis basado en el contexto que considere la información clínica proporcionada por el médico solicitante. Este enfoque garantiza que el informe sea clínicamente relevante y fácilmente comprensible, lo que ayuda a guiar las decisiones de tratamiento adecuadas.
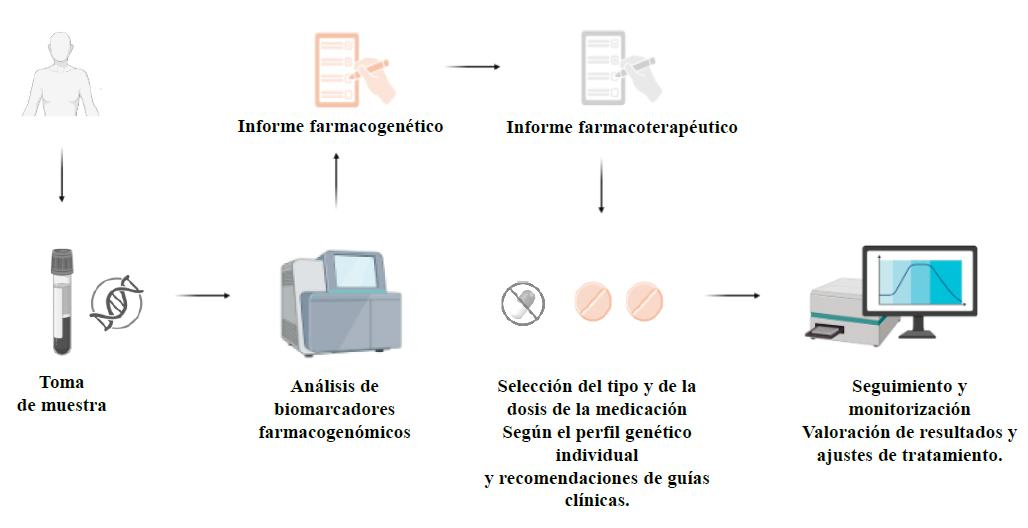
El esquema del proceso clínico se representa en la Figura 2. El proceso específico de interpretación de pruebas farmacogenéticas implica cuatro pasos consecutivos que son la detección de variantes mediante el uso de métodos de diagnóstico molecular; la caracterización del genotipo (identificación de diplotipos a partir de variantes, por ejemplo, *1/*2 y *2/*3); la vinculación de los fenotipos a partir de genotipos (por ejemplo, metabolizador normal o metabolizador lento) y finalmente la emisión del informe con las recomendaciones basadas en las guías clínicas (por ejemplo, utilizar una dosis de inicio el doble de la habitual).
Figura 2. Esquema de la dosificación individualizada de fármacos guiada por biomarcadores farmacogenómicos y posterior monitorización terapéutica. Elaboración propia. Imagen creada con BioRender.
com
Las indicaciones clínicas de las pruebas farmacogenéticas son (14):
- Variabilidad interindividual significativa en la respuesta a los fármacos.
- Rango terapéutico estrecho.
- Posibilidad de efectos adversos graves.
- Desarrollo de resistencia al tratamiento.
- Necesidad de tratamiento a largo plazo.
- Alto coste de la medicación.
Cuando se solicita al laboratorio un genotipado, el facultativo debe orientar sobre qué fármacos concretos requiere el estudio para que el laboratorio pueda emitir un informe con un contenido de mayor valor para el clínico.
Los resultados de laboratorio no pueden entregarse de forma inmediata; dependerá de la técnica. Un kit comercial basado en la reacción en cadena de la polimerasa permite al laboratorio proporcionar resultados en unos pocos días, mientras que otras técnicas, como la secuenciación de Sanger, alargan el tiempo de entrega, el cual puede superar la semana. Por ello, es importante que se establezcan los circuitos y una buena coordinación interna en el hospital para que, siempre que sea posible, se disponga del informe farmacogenético antes de empezar el tratamiento y así establecer la dosis de inicio, por ejemplo, en los pacientes trasplantados que vayan a ser tratados con tacrolimus. Uno de los factores limitantes es el tiempo necesario para realizar las determinaciones, especialmente en situaciones que puedan suponer emergencia vital (25).
Los resultados de las pruebas farmacogenéticas pueden ayudar al facultativo a reducir la incertidumbre ante casos de alto riesgo de efectos adversos o en los que hay riesgo de fracaso terapéutico. Ante los casos refractarios al tratamiento y en los que se presente toxicidad asociada a la medicación, sigue siendo imprescindible monitorizar los niveles plasmáticos del fármaco y sus metabolitos. Los resultados de la farmacocinética y farmacogenética deben ser complementarios.
Los analistas clínicos deben avisar al facultativo si la variación genética afecta a una vía que implica la metabolización de diversos fármacos, y de la necesidad de estudiar otros biomarcadores que puedan estar implicados en la cinética, transporte o acción del fármaco. En los informes emitidos es fundamental indicar en qué criterio se basa el estudio del biomarcador y utilizar siempre métodos validados.
Cabe remarcar que los resultados obtenidos de los biomarcadores analizados proporcionan una información predictiva que procede exclusivamente de información genética; la respuesta a los fármacos se ve afectada por otros factores como edad, sexo, peso, tratamientos concomitantes, enfermedades, entre otros. Por tanto, las decisiones sobre el tratamiento (modificación de dosis o cambio por un fármaco alternativo) se realizarán a criterio del médico responsable, que siempre realizará una evaluación completa del paciente, considerando todos los factores que puedan influir y no solo los genéticos.
El análisis de variantes germinales le sirve al paciente para toda la vida. Sin embargo, la interpretación puede cambiar durante el curso del seguimiento al paciente, por ejemplo, por aparición de nuevas condiciones patológicas como insuficiencia renal o hepática que puedan influir en la estrategia terapéutica a seguir.
En los hospitales, el reto actual es el desarrollo de circuitos y uso de sistemas y plataformas apropiadas; es necesaria la adecuada integración de la información farmacogenómica en la historia clínica electrónica para el apoyo a la toma de decisiones clínicas. La colaboración multidisciplinar entre los diferentes profesionales (analistas clínicos, farmacia hospitalaria, facultativos) es imprescindible para lograr los objetivos terapéuticos y la correcta interpretación del informe genético y del informe farmacoterapéutico.
6. RECURSOS ELECTRÓNICOS DE FARMACOGENÓMICA ENFOCADOS A LA PRÁCTICA CLÍNICA
Las guías son necesarias para la interpretación de las pruebas farmacogenómicas de laboratorio y así ayudar al facultativo en la toma de decisiones clínicas. Para aplicar los conocimientos de farmacogenómica, se suelen consultar diversas fuentes de información, como las guías de práctica clínica del DPWG, así como las guías PharmGKB y CPIC; estas últimas se han integrado recientemente en la base de datos ClinPGx. Las guías incluyen información detallada por genotipo, etnicidad y contexto clínico, así como las recomendaciones a seguir por el facultativo en relación con el tratamiento farmacológico.
Las combinaciones de genes y fármacos con suficiente evidencia pueden consultarse en las bases de datos CPIC y PharmGKB. Las calificaciones CPIC A y B y los niveles 1A y 1B de PharmGKB, respectivamente, indican evidencia científica suficiente para ayudar en los ajustes de dosis y predicción de toxicidad a través de pruebas farmacogenéticas.
Dentro de los recursos de farmacogenómica proporcionados por agencias reguladoras, cabe destacar las listas de biomarcadores farmacogenómicos de la FDA. Las combinaciones de genes y fármacos con suficiente evidencia se clasifican como nivel accionable en las listas de la FDA. La FDA fue la primera agencia en respaldar la incorporación de información genómica para mejorar el uso de medicamentos, proporcionando información regulatoria relativa a biomarcadores farmacogenómicos en las fichas técnicas de los medicamentos. Otras agencias como la EMA, Health Canada y la Agencia de Productos Farmacéuticos y Dispositivos Médicos de Japón (PMDA) también han integrado la farmacogenómica en su marco de evaluación de medicamentos. Así, por ejemplo, la EMA exige que se incluyan en las fichas técnicas de medicamentos aquellos datos genéticos relevantes y publica directrices sobre cómo deben incluirse datos farmacogenómicos en los ensayos clínicos y en las fichas técnicas. En este sentido, la EMA elaboró una guía de buenas prácticas en farmacogenómica, considerando que los datos genómicos son fundamentales para evaluar la eficacia y seguridad de los medicamentos en el proceso de aprobación regulatoria; la guía también proporciona orientación sobre métodos para evaluar variaciones genéticas en el ADN germinal que podrían afectar la eficacia y/o seguridad de los medicamentos (26).
6.1. Lista de biomarcadores farmacogenómicos elaborada por la FDA
La FDA ha evaluado asociaciones fármaco-gén y las ha publicado en tablas de acceso libre en su página web (27). Para estas asociaciones, la FDA considera que hay suficiente evidencia científica para sugerir que los subgrupos de pacientes con ciertas variantes genéticas o fenotipos inferidos por variantes genéticas probablemente tengan un metabolismo de medicamentos alterado y, en ciertos casos, efectos terapéuticos diferenciales, incluidas diferencias en los riesgos de eventos adversos. Si bien la FDA insiste en que la composición genética de cada paciente es solo uno de los muchos factores que pueden afectar las concentraciones y la respuesta al fármaco; destaca que la información proporcionada en estas tablas de su página web se limita únicamente a ciertas asociaciones farmacogenéticas y no proporciona la información completa necesaria para el uso seguro y eficaz de un fármaco. Por consiguiente, los profesionales sanitarios deben consultar la ficha técnica para obtener información de prescripción, incluyendo instrucciones de monitorización e información sobre otros factores que pueden afectar las concentraciones, los beneficios y los riesgos del fármaco (28).
Estas tablas sobre asociaciones farmacogenéticas elaboradas por la FDA facilitan la consulta de aquellos medicamentos que han sido aprobados en EE. UU. y contienen información farmacogenómica en su ficha técnica. Cabría diferenciar 4 grandes bloques en cuanto a información farmacogenómica recogida en la ficha técnica (29):
Indicación (selección de pacientes/eficacia): Para identificar subgrupos de pacientes a los que se debe administrar un fármaco (respondedores) o no (no respondedores). Para los pares fármaco-biomarcador de esta categoría, la ficha técnica indica que se deben realizar pruebas específicas antes de su uso. Un ejemplo de selección de pacientes es el cetuximab, que no debe utilizarse en pacientes con cáncer colorrectal cuyos tumores presentan mutaciones en el gen KRAS. Esta información aparece en la sección de indicación y se repite en otras secciones de la ficha técnica.
Seguridad: Para predecir y monitorizar reacciones adversas a medicamentos. Un ejemplo es la reducción del riesgo de hipersensibilidad al abacavir en pacientes con infección por VIH-1 portadores del alelo del antígeno leucocitario humano B*5701 (HLA-B*5701). Se recomienda el uso de este biomarcador en una advertencia destacada en la ficha técnica del medicamento que indica que el abacavir está contraindicado en pacientes con este alelo. Esta información también se incluye en las secciones de advertencias, precauciones y RAMs.
Dosificación (farmacocinética): Para predecir las dosis óptimas del fármaco, principalmente para mejorar su eficacia. Por ejemplo, los metabolizadores lentos de la warfarina (variantes CYP2C9*2 y *3) tienen menor capacidad de metabolizar la warfarina, por lo que requieren dosis más bajas. Los portadores de una variante genética (c.-1639G > A) en el gen VKORC1 (que codifica la enzima diana de la warfarina) presentan mayor sensibilidad a la warfarina, por lo que también requieren dosis más bajas. El ajuste de la dosis de warfarina según los genotipos de CYP2C9 y VKORC1 puede ayudar a optimizar la eficacia del fármaco y minimizar las RAMs.
Información: Se destaca la posible importancia clínica de los biomarcadores farmacogenéticos y se recomienda su consideración, pero no la exigencia de la prueba genética. Un ejemplo es el citalopram. La sección de farmacología clínica de la ficha técnica indica que los niveles de citalopram no mostraron diferencias significativas entre los metabolizadores lentos del CYP2D6 y los metabolizadores rápidos.
6.2. Catálogo genético del Sistema Nacional de Salud
Las pruebas genéticas y genómicas constituyen un elemento esencial para el diagnóstico y pronóstico de enfermedades de alto impacto sanitario como son las enfermedades raras y oncológicas, y la selección y el seguimiento de tratamientos óptimos. El Ministerio de Sanidad y las Comunidades Autónomas se comprometieron a incorporar las pruebas genéticas en la práctica asistencial para mejorar la precisión diagnóstica y seleccionar terapias personalizadas. Así, la cartera de servicios genómicos para el Sistema Nacional de Salud fue aprobada, en España, el 23 de junio de 2023 por el Ministerio de Sanidad y posteriormente ratificada por el Consejo Interterritorial del SNS. En 2024, se creó el Comité Asesor para la cartera común de servicios en el área de genética, adscrito a la Dirección General de Cartera Común de Servicios del Sistema Nacional de Salud y Farmacia, como el órgano coordinador entre las administraciones sanitarias implicadas en esta prestación (30). Se estima que hasta la fecha el número de pruebas genéticas aprobadas supera las 670 y cabe destacar que el sistema sanitario público español ha sido el primero en Europa en incluir la disponibilidad de algunos análisis farmacogenéticos para toda la población.
En este sentido, el Ministerio de Sanidad elabora dos bases de datos interesantes para la práctica clínica, como son el Catálogo común de pruebas genéticas y genómicas del Sistema Nacional de Salud y la Base de datos de biomarcadores farmacogenómicos. El Catálogo común de pruebas genéticas y genómicas incluye pruebas farmacogenómicas con las indicaciones dentro de la cartera común de servicios para los usuarios del SNS. Se identifican diferentes campos para cada asociación gen-fármaco: tipo de estudio genético a realizar, utilidad clínica, tipo de alteración, tipo de técnica a utilizar, tipo de muestra y el tratamiento farmacológico asociado (31).
6.3. Base de datos de biomarcadores farmacogenómicos de la Agencia Española de Medicamentos y Productos Sanitarios
En julio de 2024, la AEMPS publicó una base de datos de acceso libre con un buscador interactivo de biomarcadores farmacogenómicos con su información clínica relevante para su implementación en la práctica clínica (32). Esta base de datos permite acceder a las fichas técnicas especificando las secciones de estas que recogen la información farmacogenómica de medicamentos comercializados en España para los que existe un alto grado de evidencia para la asociación gen-implicación farmacogenética. En su primera versión, la base de datos incluyó la información farmacogenómica disponible de las asociaciones principio activo-biomarcador que, de acuerdo con los criterios establecidos por PharmGKB, presentaban un nivel de evidencia 1A. En total, se incluían 65 principios activos, asociados mayoritariamente a biomarcadores germinales, es decir, aquellos que son heredables y están presentes en todas las células del individuo. En la actualización de julio de 2025, se han añadido los principios activos asociados a biomarcadores somáticos, que son alteraciones adquiridas, presentes únicamente en determinadas células del individuo; en la actualidad, se trata fundamentalmente de biomarcadores tumorales.
Esta base de datos incluye para cada asociación, el biomarcador farmacogenómico implicado, la clase de biomarcador (germinal o somático), la información contenida en la ficha técnica, la sección en la que figura y la descripción de la relación principio activo-biomarcador. Además, se identifican aquellas asociaciones que no contienen información en ficha técnica, pero sí forman parte del Catálogo de la Cartera Común de Servicios de pruebas genéticas y genómicas, incluyendo información de acuerdo con determinadas guías clínicas.
Al igual que la FDA, la AEMPS recalca en su página web que, para su implementación, la información contenida en esta base de datos debe ser complementada con información clínica, de prescripción farmacológica y otros elementos que condicionan la variabilidad de la respuesta a fármacos; cada caso debe ser estudiado individualmente y no solo con la información contenida en esta base de datos. Específicamente, se insiste en la importancia de que los pacientes no deben ajustar su dosis de medicamento o cambiarlo por otro alternativo según la información publicada, sino que esa decisión recae solamente en el médico responsable y el equipo sanitario que le atiende.
En cuanto a la presencia de información farmacogenética relevante en las fichas técnicas de los medicamentos españoles, un estudio reciente realizado por Estévez-Paredes et al. (33) destaca que ayudaría a evitar interacciones, toxicidad o falta de eficacia terapéutica. Este estudio muestra cómo el 55,4% de las fichas técnicas incluyen información sobre biomarcadores farmacogenéticos; además, la información farmacogenómica aparece con mayor frecuencia en los grupos anatómico-terapéuticos-químicos agentes antineoplásicos e inmunomoduladores, sistema nervioso y sistema cardiovascular. Se identificaron 509 biomarcadores farmacogenéticos diferentes, de los cuales las enzimas CYP450 representaron casi el 34% del total de asociaciones fármaco-biomarcador evaluadas. De los 3679 pares fármaco-biomarcador, 102 de ellos de nivel 1A (sistema de clasificación PharmGKB). El 33,3% de estos pares fármaco-biomarcador farmacogenético se asignaron a prueba accionable, el 12,7% a prueba informativa, el 4,9% a pruebas recomendadas y el 4,9% a pruebas requeridas. Finalmente, cabe destacar que la tasa de coincidencia en el nivel de recomendación de pruebas farmacogenéticas asignado entre la AEMPS y las agencias reguladoras incluidas en la base de datos PharmGKB (es decir, la FDA, la EMA, Health Canada, la PMDA y la agencia reguladora de Suiza) osciló entre el 45% y el 65%, siendo el nivel accionable el más frecuente; por otro lado, las discrepancias entre agencias no superaron el 35% (33).
6.4. Guías del grupo de trabajo de farmacogenética holandés
El DPWG fue fundado en 2005 por la Real Asociación de Farmacéuticos Holandeses, se trata de un grupo multidisciplinar e incluye farmacéuticos clínicos, médicos, farmacólogos clínicos, químicos clínicos, epidemiólogos y toxicólogos. Los objetivos del DPWG son desarrollar recomendaciones terapéuticas (dosificación de medicamentos) basadas en farmacogenética y ayudar a los prescriptores de medicamentos y a los farmacéuticos integrando las recomendaciones en sistemas informatizados de prescripción de medicamentos y vigilancia automatizada de medicamentos (34).
6.5. Guías del CPIC
El Consorcio de Implementación de Farmacogenética Clínica se formó como un proyecto conjunto con la Red de Investigación en Farmacogenómica. Las directrices del CPIC se publican en una revista de referencia, con publicación simultánea en la base de datos ClinPGx con información/datos complementarios y actualizaciones. El objetivo del CPIC es abordar algunas de las barreras que impiden la implementación de las pruebas farmacogenéticas en la práctica clínica, como son la falta de guías de práctica clínica sobre genes y fármacos revisadas por pares, actualizadas, detalladas y de acceso libre.
El CPIC proporciona guías que permiten traducir los resultados de las pruebas de laboratorio genético en decisiones para la prescripción de fármacos específicos. Las directrices pueden centrarse en genes (p. ej., la tiopurina metiltransferasa y sus implicaciones para las tiopurinas) o en fármacos (p. ej., la warfarina y el CYP2C9 y el VKORC1) (35).
6.6. ClinPGx
Esta base de datos de acceso libre ha integrado, en 2025, entre otras, la información recogida en PharmGKB, una fuente de conocimiento farmacogenómico que abarca información clínica, incluyendo pautas de dosificación y fichas técnicas de medicamentos, asociaciones gen-fármaco relevantes para la clínica y relaciones genotipo-fenotipo. En base a la información farmacogenómica incluida en la ficha técnica por parte de las agencias reguladoras, PharmGKB establece unos criterios prácticos en cuanto a las acciones recomendadas para ese medicamento; además clasifica las pruebas farmacogenéticas en (36):
Pruebas requeridas: La ficha técnica indica que se debe realizar algún tipo de prueba de genes, proteínas o cromosomas, incluidas pruebas genéticas, ensayos de proteínas funcionales, estudios citogenéticos, etc., en el gen o producto génico antes de usar este medicamento. Este requisito puede ser solo para un subconjunto particular de pacientes.
Pruebas recomendadas: La ficha técnica indica que se recomienda realizar algún tipo de prueba de genes, proteínas o cromosomas, incluidas pruebas genéticas, ensayos de proteínas funcionales, estudios citogenéticos, etc., en el gen o producto génico antes de usar este medicamento. Es posible que esta recomendación solo sea para un subconjunto particular de pacientes.
Pruebas accionables: La ficha técnica describe un ajuste de dosis, una contraindicación o recomendación de medicamentos alternativos, u otra orientación para pacientes con un genotipo o fenotipo metabolizador en particular, si se conoce. Sin embargo, la ficha técnica no requiere ni recomienda pruebas de genotipo o fenotipo antes de usar el medicamento.
6.7. Otros recursos recomendados
La Sociedad Española de Farmacogenética y Farmacogenómica ha elaborado unas recomendaciones, de acceso libre en su página web, para promover la implementación de la farmacogenética y farmacogenómica. Su objetivo es estandarizar una serie de procedimientos que aseguren y homogenicen la calidad e interpretaciones analíticas, así como las recomendaciones clínicas asociadas en el marco de la regulación existente en España y en la Unión Europea (37). Entre otros recursos se pueden encontrar:
Recomendaciones para el uso estandarizado de términos para la redacción de informes farmacogenéticos.
Recomendaciones sobre las tecnologías para la detección de variantes farmacogenéticas.
Recomendaciones elaboradas por los grupos de trabajo para la prescripción de determinados principios activos para los cuales existen beneficios de la implementación clínica de la genotipificación.
7. CONCLUSIONES
La farmacogenómica es una rama de la medicina de precisión; esta última pretende la identificación y aplicación de la estrategia preventiva, terapéutica y diagnóstica más eficaz para cada persona. Los principales centros médicos y sistemas hospitalarios a nivel mundial están abriendo unidades de medicina de precisión para adaptar el tratamiento médico a las características individuales de cada paciente, ya sean pacientes que padecen enfermedades genéticas raras o afecciones más comunes en las que determinar las variantes genéticas ofrece la oportunidad de optimizar el balance beneficio/riesgo del tratamiento farmacológico.
La información farmacogenómica es evaluada por las agencias reguladoras del medicamento, y se encuentra disponible en las fichas técnicas de los medicamentos autorizados, por ejemplo, medicamentos aprobados por la Agencia Europea del Medicamento y por la FDA. Guías como las del CPIC y recursos como ClinPGx facilitan la prescripción basada en genética.
Actualmente, la integración de pruebas farmacogenéticas en la práctica clínica está respaldada por una evidencia científica sólida y está facilitada por su menor coste. Cabe resaltar que, en España, determinadas pruebas farmacogenéticas están ya incluidas dentro de la cartera de servicios del Sistema Nacional de Salud y se están ofreciendo en hospitales públicos.
Con el análisis de biomarcadores farmacogenéticos se pretende incrementar la efectividad del tratamiento y/o reducir la toxicidad inducida por ciertos medicamentos. Esto se logra mediante informes farmacogenéticos y farmacoterapéuticos que permiten orientar al facultativo sobre si es necesario llevar a cabo un ajuste de dosis o un cambio de opción terapéutica según el genotipo del paciente. Posteriormente, se debe realizar el seguimiento y la monitorización terapéutica del paciente para asegurar que se están produciendo los resultados esperados en salud.
La aplicación de la farmacogenética depende de equipos multidisciplinares de médicos, farmacéuticos, genetistas, bioinformáticos y otros profesionales de la salud, que puedan analizar el perfil genético e integrar todos los datos con el fin de traducir la evidencia disponible en recomendaciones farmacológicas. Los softwares y algoritmos de inteligencia artificial pueden ser de utilidad para integrar información de las complejas interacciones que existen entre el genotipo, los parámetros clínicos, el estilo de vida y la exposición a factores ambientales, facilitando la toma de decisiones clínicas para una adecuada individualización del tratamiento.
Es preciso adaptar el marco legal existente para regular las pruebas genéticas que se comercializan directamente al consumidor, así como la inteligencia artificial y el aprendizaje automático con fines sanitarios. La ausencia de una legislación clara y armonizada sobre las pruebas genéticas directas al consumidor puede suponer un riesgo para las personas, en especial cuando se realizan fuera del entorno sanitario.
Conflicto de intereses
La autora declara que no existe ningún conflicto de interés.
Financiación
Este trabajo no ha recibido ninguna subvención de agencias públicas, ni financiación del sector privado ni ayuda de entidades sin fines de lucro.
Agradecimientos
Mi agradecimiento a aquellas personas que a lo largo de mi vida me han apoyado, sin cuya ayuda hoy no habría sido quien soy ni alcanzado el lugar profesional que ocupo.
8. REFERENCIAS
- Ayuso García C. Genética clínica. En: Bases de la terapéutica medicamentosa. Madrid: Consejo General de Colegios Oficiales de Farmacéuticos; 2023. p. 127-148.
- Genetic Alliance. The New York-Mid-Atlantic Consortium for Genetic and Newborn Screening Services. Understanding Genetics: A New York, Mid-Atlantic Guide for Patients and Health Professionals. Washington (DC): Genetic Alliance; 2009 Jul 8. PMID: 23304754.
- Floris M, Cano A, Porru L, Addis R, Cambedda A, Idda ML, et al. Direct-to-Consumer Nutrigenetics Testing: An Overview. Nutrients. 2020 Feb 21; 12(2):566. doi: 10.3390/nu12020566.
MedlinePlus [Internet]. ¿Qué son los estudios de asociación de genoma completo? [Citado 29 Jun 2025]. Disponible en: https://medlineplus.gov/spanish/genetica/entender/investigaciongenomica/estudiosgenomacompleto/ - National Human Genome Research Institute. Regulation of Genetic Tests [Internet]. [Citado 29 Jun 2025]. Disponible en: https://www.genome.gov/about-genomics/policy-issues/Regulation-of-Genetic-Tests
- Agencia Española de Medicamentos y Productos Sanitarios. Terapias avanzadas [Internet]. [Citado 29 Jun 2025]. Disponible en: https://www.aemps.gob.es/medicamentos-de-uso-humano/medicamentos-de-fabricacion-no-industrial/terapias-avanzadas/
- Maroñas Amigo O, Gil Rodríguez A, Carracedo Álvarez AM. Farmacogenética en oncología. En: Farmacología y farmacoterapia de las patologías oncológicas. Madrid: Consejo General de Colegios Oficiales de Farmacéuticos. 2024. p. 31-47.
- ClinPGx [Internet]. [Citado 29 Jun 2025]. Disponible en: https://www.clinpgx.org/
- Swen JJ, van der Wouden CH, Manson LE, Abdullah-Koolmees H, Blagec K, Blagus T, et al; Ubiquitous Pharmacogenomics Consortium. A 12-gene pharmacogenetic panel to prevent adverse drug reactions: an open-label, multicentre, controlled, cluster-randomised crossover implementation study. Lancet. 2023 Feb 4; 401(10374):347-356. doi: 10.1016/S0140-6736(22)01841-4. Erratum in: Lancet. 2023 Aug 26;402(10403):692. doi: 10.1016/S0140-6736(23)01742-7.
- Carracedo A, Lamas MJ. Farmacogenética y farmacogenómica. Sociedad Española de Farmacia Hospitalaria.[Internet]. Disponible en: ttps://gruposdetrabajo.sefh.es/pkgen/images/stories/modulo1_tema1.pdf
- Nunez-Torres R, Pita G, Peña-Chilet M, López-López D, Zamora J, Roldán G, et al. A Comprehensive Analysis of 21 Actionable Pharmacogenes in the Spanish Population: From Genetic Characteriation to Clinical Impact. Pharmaceutics. 2023; 15(4):1286. doi.org/10.3390/pharmaceutics15041286
- Fundación Instituto Roche. Farmacogenómica: el camino hacia la personalización del tratamiento. [Internet]. 2021 [citado 29 Jun 2025]. Disponible en: https://www.institutoroche.es/static/pdfs/Informes_anticipando_2021_FARMACOGENOMICA_WEB.pdf
- Sociedad Española de Farmacia Hospitalaria. Farmacogenética y procesos ADME. [Internet]. Disponible en: https://gruposdetrabajo.sefh.es/pkgen/images/stories/modulo1_tema2.pdf
- Rim JH, Kim YG, Kim S, Choi R, Lee JS, Park S, et al; Pharmacogenetics Guideline Task-Force Team of the Korean Society for Laboratory Medicine. Clinical Pharmacogenetic Testing and Application: 2024 Updated Guidelines by the Korean Society for Laboratory Medicine. Ann Lab Med. 2025 Mar 1; 45(2):121-132. doi: 10.3343/alm.2024.0572.
- Cavallari LH, Hicks JK, Patel JN, Elchynski AL, Smith DM, Bargal SA, et al. The Pharmacogenomics Global Research Network Implementation Working Group: global collaboration to advance pharmacogenetic implementation. Pharmacogenet Genomics. 2025 Jan 1; 35(1):1-11. doi: 10.1097/FPC.0000000000000547.
- Taherdoost H, Ghofrani A. AI’s role in revolutionizing personalized medicine by reshaping pharmacogenomics and drug therapy. Intelligent Pharmacy. 2024. 2(5):643-650. doi.org/10.1016/j.ipha.2024.08.005.
- Morris SA, Alsaidi AT, Verbyla A, Cruz A, Macfarlane C, Bauer J, et al. Cost Effectiveness of Pharmacogenetic Testing for Drugs with Clinical Pharmacogenetics Implementation Consortium (CPIC) Guidelines: A Systematic Review. Clin Pharmacol Ther. 2022 Dec; 112(6):1318-1328. doi: 10.1002/cpt.2754.
- Plöthner M, Ribbentrop D, Hartman JP, Frank M. Cost-effectiveness of pharmacogenomic and pharmacogenetic test-guided personalized therapies: A systematic review of the approved active substances for personalized medicine in Germany. Advances in Therapy. 2016. 33(9): 1461-80. doi: https://doi.org/10.1007/s12325-016 0376-8.
- David V, Fylan B, Bryant E, Smith H, Sagoo GS, Rattray M. An Analysis of Pharmacogenomic-Guided Pathways and Their Effect on Medication Changes and Hospital Admissions: A Systematic Review and Meta-Analysis. Front Genet. 2021 Jul 30; 12:698148. doi: 10.3389/fgene.2021.698148.
- Pratt VM, Cavallari LH, Fulmer ML, Gaedigk A, Hachad H, Ji Y, et al. TPMT and NUDT15 Genotyping Recommendations: A Joint Consensus Recommendation of the Association for Molecular Pathology, Clinical Pharmacogenetics Implementation Consortium, College of American Pathologists, Dutch Pharmacogenetics Working Group of the Royal Dutch Pharmacists Association, European Society for Pharmacogenomics and Personalized Therapy, and Pharmacogenomics Knowledgebase. J Mol Diagn. 2022 Oct; 24(10):1051-1063. doi: 10.1016/j.jmoldx.2022.06.007.
- Montero-Gómez A, Sánchez Pozo A. Selección de variantes farmacogenómicas y metodología para su uso en farmacia comunitaria. Farm Comunitarios. 2024 Sep 17; 16(4):61-82. doi: 10.33620/FC.2173-9218. (2024).27.
- Sociedad Española de Farmacia Hospitalaria. Notas de Prensa. En el 60% de los hospitales los especialistas en Farmacia Hospitalaria realizan la recomendación farmacoterapéutica tras la determinación genética [Internet] [Actualizado 27 Ene 2025; citado 30 Jun 2025]. Disponible en: https://www.sefh.es/sefh-sala-prensa/noticia/1826
- Carter JL, Critchlow J, Jackson S, Sanghvi S, Feger H, Chaudhry A, et al. Pharmacogenomic alerts: Developing guidance for use by healthcare professionals. Br J Clin Pharmacol. 2022 Jul; 88(7):3201-3210. doi: 10.1111/bcp.15234.
- Hospital General Universitario Gregorio Marañón. Monitorización farmacogenética [Internet]. [Citado 9 Nov 2025]. Disponible en: https://www.comunidad.madrid/hospital/gregoriomaranon/profesionales/monitorizacion-farmacogenetica
- Hospital Universitario Son Espases. I Jornada Balear de Farmacogenética: De la teoría a la práctica. 10 Abr 2025. [Citado 28 Jun 2025]
- European Medicines Agency. Good pharmacogenomic practice – Scientific guideline [Internet]. [Actualizado 13 Jul 2018; citado 25 Jun 2025]. Disponible en: https://www.ema.europa.eu/en/good-pharmacogenomic-practice-scientific-guideline
- Food and Drug Administration [Internet]. Table of Pharmacogenomic Biomarkers in Drug Labeling. [Actualizado 23 Sep 2024; citado 28 Jun 2025]. Disponible en: https://www.fda.gov/drugs/science-and-research-drugs/table-pharmacogenomic-biomarkers-drug-labeling
- Food and Drug Administration [Internet]. Table of Pharmacogenetic Associations. [Actualizado 26 Oct 2022; citado 28 Jul 2025]. Disponible en: https://www.fda.gov/medical-devices/precision-medicine/table-pharmacogenetic-associations
- Mehta D, Uber R, Ingle T, Li C, Liu Z, Thakkar S, et al. Study of pharmacogenomic information in FDA-approved drug labeling to facilitate application of precision medicine. Drug Discov Today. 2020 May; 25(5):813-820. doi: 10.1016/j.drudis.2020.01.023.
- Ministerio de Sanidad. Orden SND/606/2024, de 13 de junio, por la que se crea el Comité Asesor para la Cartera Común de Servicios en el Área de Genética, y por la que se modifican los anexos I, II, III, VI y VII del Real
- Decreto 1030/2006, de 15 de septiembre, por el que se establece la cartera de servicios comunes del Sistema Nacional de Salud y el procedimiento para su actualización. BOE núm 147, de 18 de junio de 2024, págs. 70588–70609.
- Ministerio de Sanidad. Catálogo Común de Pruebas Genéticas y Genómicas [Internet]. [Citado 31 Jun 2025]. Disponible en: https://cgen.sanidad.gob.es/#/
- Agencia Española de Medicamentos y Productos Sanitarios (AEMPS). Base de datos de biomarcadores farmacogenómicos [Internet]. [Citado 28 jul 2025]. Disponible en: https://www.aemps.gob.es/medicamentos-de-uso-humano/base-de-datos-de-biomarcadores-farmacogenomicos/
- Estévez-Paredes M, Mata-Martín MC, de Andrés F, Llerena A. Pharmacogenomic biomarker information on drug labels of the Spanish Agency of Medicines and Sanitary products: evaluation and comparison with other regulatory agencies. Pharmacogenomics J. 2024 Jan 17; 24(1):2. doi: 10.1038/s41397-023-00321-y.
- ClinPGx. DPWG: Dutch Pharmacogenetics Working Group [Internet]. [Citado 30 Jun 2025]. Disponible en: https://www.pharmgkb.org/page/dpwg#dpwg-publications
- Pharmacogenomics Research Network (PGRN). PGRN Resources [Internet]. [Citado 30 Jun 2025]. Disponible en: https://www.pgrn.org/pgrn-resources
- The Pharmacogenomics Knowledgebase (PharmGKB) [Internet]. [Citado 27 Jun 2025]. Disponible en: https://www.pharmgkb.org/about
- Sociedad Española de Farmacogenética y Farmacogenómica (SEFF). Recomendaciones de los grupos de trabajo de la SEFF [Internet]. [Citado 28 Jun 2025]. Disponible en: https://seff.es/recomendaciones-grupos-de-trabajo-de-la-seff/